Ryhmä 14: Yleiset ominaisuudet ja reaktiot
Hiili
Hiili on maan neljänneksi yleisin alkuaine. Se on erityisen kiinnostava orgaanisessa kemiassa, koska se on orgaanisen yhdisteen erottava piirre. Sitä pidetään myös biologian ”selkärangana”, koska kaikki maapallon elämänmuodot perustuvat hiileen. Tämä johtuu kahdesta hiilen tärkeästä ominaisuudesta: sen pienestä koosta ja ainutlaatuisesta elektronikonfiguraatiosta. Koska hiiliatomit ovat pieniä, niiden p-orbitaalielektronit menevät päällekkäin ja mahdollistavat π-sidosten muodostumisen. Vertaa alla olevia CO2: n ja SiO2: n molekyylirakenteita:
Hiilen elektronikonfiguraatio antaa sen muodostaa erittäin vakaita sidoksia happi ja vety. Nämä sidokset varastoivat valtavan määrän energiaa. Näiden sidosten muodostuminen (kiinnittyminen) ja rikkoutuminen (palaminen) hiilen kierrossa helpottavat maallista elämää:
- Hiilen kiinnitys: fotosynteesissä kasvit käyttävät aurinkoenergiaa ja klorofyllimolekyylejä muuttamaan ilmakehän kaasumaista hiilidioksidia yksinkertaisiksi hiilihydraateiksi, kuten glukoosiksi:
\
- Hiilen palaminen: Aerobisessa hengityksessä kasvit ja eläimet hajottavat hiilihydraatit hiilidioksidiksi ja vedeksi (kuten alla olevassa yhtälössä on esitetty) ja käyttävät vapautunutta energiaa polttoaineen biologiseen toimintaan – kasvuun , liikkuminen jne. Lisäksi fossiilisten polttoaineiden sisältämien hiilihydraattien palaminen antaa nykyajan toimintaan tarvittavaa energiaa.
\
Rikin vieressä hiili on eniten allotrooppisia aineita. Hiilellä on kolme pääasiallista kiinteän tilan allotrooppia: grafiitti, timantti ja fullereenit (joista tunnetuin, buckminsterfullerene, tunnetaan myös nimellä ”buckyball”). Nämä allotroopit eroavat toisistaan suuresti, mutta niitä käytetään laajasti modernissa tuotannossa.
Grafiitti ja timantti
Grafiitilla on voiteluominaisuuksia, jotka tekevät siitä erittäin sopivan käytettäväksi lyijykynissä. Koska se koostuu kuusijäsenisten renkaiden tasoista, jotka voivat helposti liukua toistensa ohitse, grafiitti liukuu helposti ja sitä käytetään siksi yhdessä saven kanssa lyijykynän ”lyijyn” muodostamiseksi. Grafiittia käytetään myös kuitumaisessa muodossa erilaisiin muoveihin.
Hiilellä on erittäin korkeat sulamis- ja kiehumispisteet. Grafiitti on termodynaamisesti vakain hiilen allotrooppi tavallisissa olosuhteissa. Timantissa, vakaammassa allotroopissa äärimmäisissä paineissa (105 atm ja ylöspäin), kukin hiiliatomi on sitoutunut neljään muuhun tetraedraalisessa järjestelyssä, jolloin tuloksena on vaikein luonnossa esiintyvä aine. Tämä kovuus yhdistettynä hyvään kykyyn johtaa lämpöä tekee timantista ja timanttikalvosta erinomaiset materiaalit poranterissä ja muissa koneen osissa; Laadukkaimpia luonnon timantteja käytetään kuitenkin pääasiassa koruihin, kun taas alempilaatuisia timantteja tai jopa synteettisiä timantteja käytetään teollisiin tarkoituksiin.
Fullerenes (nimetty R. Buckminster Fullerin mukaan) ja nanoputket ovat sarja hiilialotrooppien, joissa hiilirenkaat muodostavat monimutkaisempia muotoja, mukaan lukien jalkapallomaiset molekyylit (C60) ja kanalangasta valmistetut sylinterit. Grafeeni, yksi hiililevy, jolla on kiehtovat elektroniset ominaisuudet, on näiden allotrooppien perusta. Fullereeneja esiintyy, kun tietty prosenttiosuus kuusikulmaisia renkaita on koottu muodostamaan viisikulmaisia renkaita, mikä saa levyn vääntymään karkeasti pallomaiseksi ”Buckyballiksi”. Hiilinanoputki on yksinkertaisesti grafeeni taivutettu sylinteriksi. Jotkut näistä allotroobeista muodostuvat grafiitin hajoamisessa. Palaminen voi myös tuottaa vaihtoehtoisia hiilimuotoja. Lämmitetty hiili ilman ilmaa muodostaa koksin. Vastaavasti lämmitetystä puusta tulee hiiltä, kun haihtuvat integroidit pakotetaan pois.

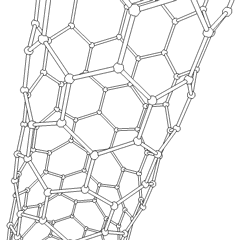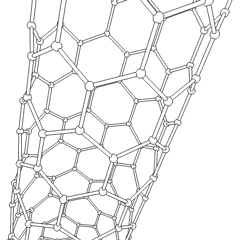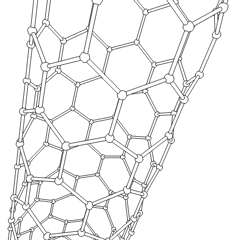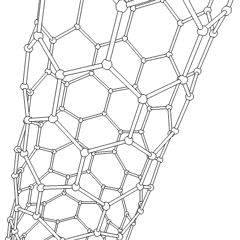
On lähes lukemattoman määrän erilaisia hiiliyhdisteitä, mutta useat epäorgaaniset yhdisteet ovat erityisen tärkeitä. Hiilimonoksidia (CO) käytetään muiden hiiliyhdisteiden syntetisointiin, metalliyhdisteiden pelkistämiseen käyttökelpoisiksi tuotteiksi ja yhdessä muiden polttoaineiden kaasujen kanssa. Karbideja, hiiliyhdisteitä ja metalleja käytetään monissa teollisissa prosesseissa, usein muiden metallirakenteiden stabiloimiseksi; kalsiumkarbidia käytetään esimerkiksi teollisten kemiallisten yhdisteiden valmistamiseen. Hiilidisulfidi ja hiilitetrakloridi ovat voimakkaita liuottimia (vaikka CCl4: n käyttö on vähentynyt karsinogeeniksi luokittelun jälkeen). Syanidi käyttäytyy samalla tavalla kuin halogenidi-ionit muodostaen sekä suolan että hapon. Syaanivetyhappo (HCN) on heikko happo, jolla on erittäin alhainen kiehumispiste (itse asiassa huoneenlämpötila), ja sitä käytetään muovituotannossa.Syanididimeeriä kutsutaan syanogeeniksi, ja sitä käytetään orgaanisissa synteeseissä, fumiganteissa ja rakettiajossa.