Renoveret C-T-celleterapi reducerer bivirkninger i første kliniske forsøg
20. februar 2020 af NCI-personale
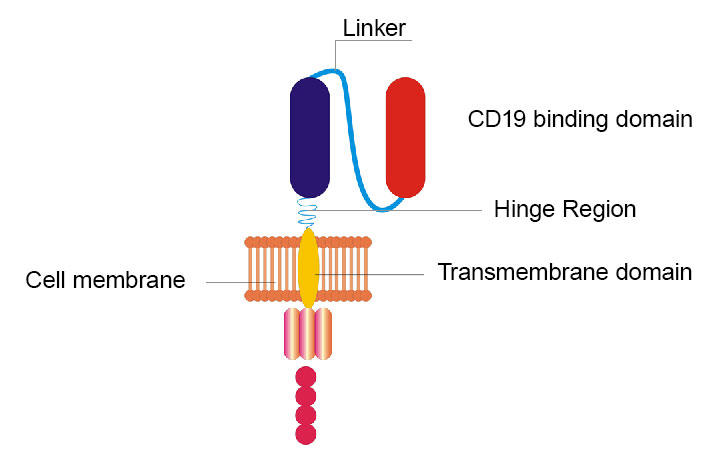
NCI-forskere ombyggede deres originale CD19 CAR ved at udskifte hængslet og transmembrane domæner og bytte af CD19-bindingsdomænet fra et proteinfragment fundet hos mus til et lignende fragment fundet hos mennesker.
I løbet af flere årtier lagde NCI-videnskabsmænd et omfattende fundament for en roman behandling, der til sidst fortsætter med at blive axicabtagene ciloleucel (Yescarta), en CAR T-cellebehandling for voksne med lymfom.
Selvom terapien kan føre til langvarige remissioner hos nogle patienter med meget avanceret kræft, kan den også forårsage neurologiske bivirkninger såsom taleproblemer, rysten, delirium og kramper. Nogle bivirkninger kan være alvorlige eller fatale.
Så i 2017 tilpassede NCI-forskere deres oprindelige CAR T-celle-design med det mål at skabe en mere sikker og mere effektiv terapi. Nu viser resultater fra det første kliniske forsøg med de ombyggede CAR T-celler, at de måske har nået en del af deres mål.
Den nye terapi forårsagede langt færre neurologiske bivirkninger end den oprindelige terapi gjorde i et tidligere forsøg, alligevel var det lige så effektivt. Resultaterne blev rapporteret den 20. januar i Nature Medicine.
“Det er bemærkelsesværdigt, at ud af 20 patienter i dette forsøg havde kun én alvorlige neurologiske bivirkninger,” sagde associeret efterforsker Jennifer Brudno, MD, fra NCIs Center for Kræftforskning.
“Dette ser ud til at være et betydeligt fremskridt i vores nuværende forståelse af, hvordan CAR T-celler fungerer, og hvordan man laver en mere sikker CAR T,” siger David Maloney, MD, Ph.D., medicinsk direktør for cellulær immunterapi for Fred Hutchinson Cancer Research Center, som ikke var involveret i undersøgelsen.
Undersøgelsen er dog begrænset af det lille antal involverede patienter, og den relativt korte tid, hvor patienternes resultater er blevet sporet, tilføjede han.
T-celler får en ny BIL
BIL T-cellebehandling involverer tilkobling af en patients egne T-celler (en type hvide blodlegemer) med et specialiseret protein kaldet CAR eller kimærisk antigenreceptor. Denne receptor hjælper T-cellerne med at finde og dræbe personens kræft.
NCI-holdets ombyggede CAR adskiller sig fra originalen på få måder. For eksempel blev to sektioner (kaldet hængsel og transmembrane domæner) af den originale CAR udskiftet. Og et andet afsnit, der oprindeligt bestod af et proteinfragment, der blev fundet hos mus, blev byttet mod et lignende fragment, der blev fundet hos mennesker. Men ligesom originalen retter den nye CAR sig også mod CD19, et molekyle der studer overfladen af lymfomceller.
I tidligere laboratorieundersøgelser fandt forskerne, at T-celler bevæbnet med den nye CAR bremsede væksten af tumorer hos mus. Og sammenlignet med de originale CAR T-celler, producerede de nye CAR T-celler lavere niveauer af stoffer kaldet cytokiner.
Forskere forstår ikke fuldt ud, hvordan CAR T-celler forårsager neurologiske bivirkninger, men cytokiner kan delvis være bebrejde. Cytokiner er også synderen for cytokinfrigivelsessyndrom, en anden potentielt livstruende bivirkning af CAR T-cellebehandling.
Med disse lovende resultater gik teamet fremad med en første-i-menneskelig undersøgelse af de ombyggede CAR T-celler.
Færre cytokiner, færre neurologiske bivirkninger
I det nye forsøg gav Dr. Brudno og hendes kolleger den nye CAR T-cellebehandling til 20 patienter med B-celle lymfom.
Samlet set oplevede fire patienter (20%) en vis neurologisk toksicitet: Tre havde milde virkninger, og en (5%) oplevede alvorlige virkninger, der hurtigt forsvandt efter behandling med et steroid (medicin, der dæmper immunsystemet ).
I en tidligere undersøgelse af den originale CAR T-cellebehandling, der involverede 22 personer med B-celle lymfom, oplevede 17 (77%) en vis neurologisk toksicitet – inklusive 11 patienter (50%), der oplevede alvorlige symptomer.
To patienter (10%) i det nye forsøg og fire (18%) i det tidligere forsøg havde svær cytokinfrigivelsessyndrom. “Det synes gunstigt, at lignende, men det er vanskeligt at sige, om det bestemt er mindre hyppigt” med den nye terapi, sagde Dr. Brudno.
Cytokinniveauet var lavere i blodet hos patienter, der blev behandlet med den nye terapi. end hos patienter, der fik den originale terapi, fandt forskerne, hvilket kan forklare, hvorfor den nye terapi forårsagede færre neurologiske bivirkninger, skrev de.
I begge forsøg brugte forskerne de samme metoder til at klassificere sværhedsgraden. af neurologisk toksicitet og cytokinfrigivelsessyndrom, bemærkede Dr. Brudno.
Og selv om der er andre ligheder mellem de to forsøg – for eksempel blev de udført på samme anlæg – det er vanskeligt at sammenligne resultater fra uafhængige undersøgelser, sagde hun.
CAR T-celler, der holder fast
Et problem med de nuværende CAR T-celleterapier er, at cellerne ikke holder meget længe i patientens krop. Det skyldes delvis, at det humane immunsystem kan se museproteiner som ukendte og ødelægge CAR T-cellerne.
En del af holdets mål var at oprette CAR T-celler, der holder sig fast eller vedvarer længere. De begrundede, at T-celler med en CAR fremstillet af alle humane proteiner muligvis varer længere end celler med en CAR, der indeholder museproteiner.
Hvis patientens immunsystem ignorerer en CAR fremstillet af humane proteiner, kan CAR T-cellerne muligvis vare længere og være mere effektive, forklarede Dr. Brudno.
Det kan være tilfældet til den nye terapi. En måned efter modtagelse af behandlingen var der højere niveauer af CAR T-celler i blodet hos patienter, der fik den nye terapi end hos dem, der blev behandlet med den oprindelige behandling.
Disse fund er “opmuntrende” og bør være undersøgt i fremtidige undersøgelser, sagde Dr. Maloney.
Selvom de nye CAR T-celler ser ud til at vare længere end de originale CAR T-celler, så de ikke ud til at være mere effektive. I begge forsøg var mere end halvdelen (55%) af deltagerne gik i fuldstændig remission.
Men det er “opmuntrende” at se “meget god effekt for dette CAR T-celleprodukt ud over den lave toksicitet,” Dr. Brudno sagde.
En informativ redesign
BIL-T-cellebehandling kan føre til en bred vifte af neurologiske effekter, der spænder fra meget mild til svær og livstruende, forklarede Dr. Brudno.
Disse bivirkninger er forbundet med alle aktuelt tilgængelige CAR T-celle-terapier – to, der er FDA-godkendte, og en anden, indtil FDA-godkendelse afventer – bemærkede dr. Maloney. udies, har antallet af alvorlig neurologisk toksicitet varieret fra 5% til 50%.
Andre kliniske forsøg tester CAR T-celleterapier, der også er blevet redesignet til at være mere sikre, bemærkede Dr. Maloney. Den nye NCI-undersøgelse identificerer aspekter af CAR T-celle-design, der ikke tidligere var kendt for at påvirke neurologisk toksicitet, sagde han.
“Men hvordan man oversætter det til et nyt kommercielt produkt eller opgraderer kommercielt produkt er et helt andet spørgsmål,” sagde han. Fremstilling af en CAR T-cellebehandling til hver enkelt patient er en kompleks og dyr proces, der kan kun udføres på højt specialiserede faciliteter.
For nu er NCI-teamet, ledet af James Kochenderfer, MD, fokuseret på at udføre kliniske forsøg med forskellige CAR T-cellebehandlinger til mennesker med en anden type blod kræft, myelomatose.