Ombygd C-T-celleterapi reduserer bivirkninger i første kliniske studie
20. februar 2020, av NCI Staff
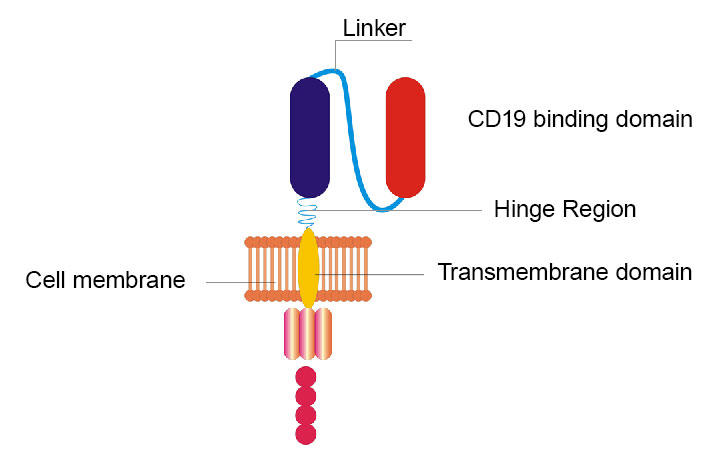
NCI-forskere ombygde sin opprinnelige CD19 CAR ved å erstatte hengslet og transmembrane domener og bytte CD19-bindingsdomenet fra et proteinfragment funnet hos mus til et lignende fragment funnet hos mennesker.
I løpet av flere tiår la NCI-forskere omfattende grunnlag for en roman behandling som til slutt vil fortsette å bli axicabtagene ciloleucel (Yescarta), en CAR T-cellebehandling for voksne med lymfom.
Selv om behandlingen kan føre til langvarige remisjoner for noen pasienter med svært avansert kreft, kan den også forårsake nevrologiske bivirkninger som taleproblemer, skjelving, delirium og kramper. Noen bivirkninger kan være alvorlige eller dødelige.
Så i 2017 justerte NCI-forskere sin opprinnelige CAR T-celle-design med mål om å skape en tryggere og mer effektiv terapi. Nå antyder resultater fra den første kliniske studien av de ombygde CAR T-cellene at de kan ha oppnådd en del av målet.
Den nye behandlingen forårsaket langt færre nevrologiske bivirkninger enn den opprinnelige behandlingen gjorde i en tidligere studie, likevel var det like effektivt. Funnene ble rapportert 20. januar i Nature Medicine.
«Det er bemerkelsesverdig at av en 20 pasienter i denne studien hadde bare én alvorlige nevrologiske bivirkninger,» sa assisterende etterforsker Jennifer Brudno, MD, ved NCIs Center for Cancer Research.
«Dette ser ut til å være et betydelig fremskritt i vår nåværende forståelse av hvordan CAR T-celler fungerer og hvordan vi kan lage en tryggere CAR T,» sa David Maloney, MD, Ph.D., medisinsk direktør for cellulær immunterapi for Fred Hutchinson Cancer Research Center, som ikke var involvert i studien.
Studien er imidlertid begrenset av det lille antallet pasienter som er involvert, og den relativt korte tiden pasientenes resultater har blitt sporet, la han til.
T-celler får en ny BIL
BIL-T-cellebehandling innebærer tilkobling av pasientens egne T-celler (en type hvite blodlegemer) med et spesialisert protein kalt CAR, eller kimært antigenreseptor. Denne reseptoren hjelper T-cellene med å finne og drepe kreft hos personen.
NCI-teamets ombygde BIL er forskjellig fra originalen på noen få måter. For eksempel ble to seksjoner (kalt hengsel og transmembrane domener) av den opprinnelige CAR erstattet. Og en annen seksjon som opprinnelig besto av et proteinfragment som ble funnet hos mus, ble byttet mot et lignende fragment som ble funnet hos mennesker. Men i likhet med originalen retter den nye bilen seg også mot CD19, et molekyl som studer overflaten av lymfomceller.
I tidligere laboratoriestudier fant forskerne at T-celler bevæpnet med den nye CAR bremset veksten av svulster hos mus. Og sammenlignet med de originale CAR T-cellene, produserte de nye CAR T-cellene lavere nivåer av stoffer som kalles cytokiner.
Forskere forstår ikke helt hvordan CAR T-celler forårsaker nevrologiske bivirkninger, men cytokiner kan være delvis til skylde på. Cytokiner er også synderen for cytokinfrigivelsessyndrom, en annen potensielt livstruende bivirkning av CAR T-cellebehandling.
Med disse lovende resultatene gikk teamet videre med en første-i-menneskelig studie av de ombygde CAR T-cellene.
Færre cytokiner, færre nevrologiske bivirkninger
I den nye studien ga Dr. Brudno og hennes kolleger den nye CAR T-celleterapien til 20 pasienter med B-celle lymfom.
Totalt sett opplevde fire pasienter (20%) noe nevrologisk toksisitet: Tre hadde milde effekter og en (5%) opplevde alvorlige effekter som raskt forsvant etter behandling med et steroid (medisin som tapper immunforsvaret ).
I en tidligere studie av den opprinnelige CAR T-celleterapien som involverte 22 personer med B-celle lymfom, opplevde 17 (77%) noe nevrologisk toksisitet – inkludert 11 pasienter (50%) som opplevde alvorlige symptomer.
To pasienter (10%) i den nye studien og fire (18%) i den tidligere studien hadde alvorlig cytokinfrigivelsessyndrom. «Det virker gunstig at lignende, men det er vanskelig å si om det definitivt er mindre hyppig» med den nye behandlingen, sa Dr. Brudno.
Cytokinnivået var lavere i blodet hos pasienter som ble behandlet med den nye behandlingen. enn hos pasienter som fikk den opprinnelige behandlingen, fant forskerne, noe som kan forklare hvorfor den nye behandlingen forårsaket færre nevrologiske bivirkninger, skrev de.
I begge forsøkene brukte forskerne de samme metodene for å gradere alvorlighetsgraden. av nevrologisk toksisitet og cytokinfrigivelsessyndrom, bemerket Dr. Brudno.
Og selv om det er andre likheter mellom de to forsøkene – for eksempel ble de utført på samme anlegg – det er vanskelig å sammenligne resultater fra uavhengige studier, sa hun.
CAR T-celler som holder seg rundt
Et problem med dagens CAR T-cellebehandlinger er at cellene ikke varer veldig lenge i pasientens kropp. Det er delvis fordi det menneskelige immunforsvaret kan se museproteiner som ukjente og ødelegge CAR T-celler.
En del av teamets mål var å lage CAR T-celler som holder seg, eller vedvarer, lenger. De resonnerte at T-celler med en CAR laget av alle humane proteiner kan vare lenger enn celler med en CAR som inneholder museproteiner.
Hvis pasientens immunsystem ignorerer en BIL laget av humane proteiner, kan CAR T-cellene vare lenger og være mer effektive, forklarte Dr. Brudno.
Det kan være tilfelle for den nye terapien. En måned etter mottak av behandlingen var det høyere nivåer av CAR T-celler i blodet fra pasienter som fikk den nye behandlingen enn hos de som ble behandlet med den opprinnelige behandlingen.
Disse funnene er «oppmuntrende» og bør være utforsket i fremtidige studier, sa Dr. Maloney.
Selv om de nye CAR T-cellene ser ut til å vedvare lenger enn de originale CAR T-cellene, så de ikke ut til å være mer effektive. I begge forsøkene var mer enn halvparten (55%) av deltakerne gikk i fullstendig remisjon.
Men det er «oppmuntrende» å se «veldig god effekt for dette CAR T-celleproduktet, i tillegg til den lave toksisiteten,» Dr. Brudno sa.
En informativ redesign
BIL-T-cellebehandling kan føre til et mangfoldig utvalg av nevrologiske effekter, alt fra veldig mild til alvorlig og livstruende, forklarte Dr. Brudno.
Disse bivirkningene er assosiert med alle tilgjengelige CAR T-celle-terapier – to som er godkjent av FDA og en annen i påvente av FDA-godkjenning – bemerket dr. Maloney. udies, har frekvensen av alvorlig nevrologisk toksisitet vært i området fra 5% til 50%.
Andre kliniske studier tester CAR T-celleterapier som også har blitt redesignet for å være tryggere, bemerket Dr. Maloney. Den nye NCI-studien identifiserer aspekter av CAR T-celle-design som ikke tidligere var kjent for å påvirke nevrologisk toksisitet, sa han.
«Men hvordan du oversetter det til et nytt kommersielt produkt eller oppgraderer kommersielt produkt er et helt annet spørsmål,» sa han. Å produsere en CAR T-cellebehandling for hver enkelt pasient er en kompleks og kostbar prosess som kan bare gjøres på høyspesialiserte fasiliteter.
Foreløpig er NCI-teamet, ledet av James Kochenderfer, MD, fokusert på å gjennomføre kliniske studier av forskjellige CAR T-celleterapier for personer med en annen type blod kreft, myelomatose.