9.9 En introduksjon til organisk syntese
Mål
Etter å ha fullført dette avsnittet, bør du kunne utforme en flerstegssyntese å forberede et gitt produkt fra et gitt utgangsmateriale ved å bruke noen av reaksjonene som ble introdusert i læreboka fram til dette punktet.
Studienoter
Du bør har lagt merke til at noen av de tildelte problemene har krevd at du strenger sammen et antall organiske reaksjoner for å konvertere en organisk forbindelse til en annen når det ikke er noen eneste reaksjon for å nå dette målet. En slik rekke reaksjoner kalles en «organisk syntese.» Et av hovedmålene med dette kurset er å hjelpe deg med å designe slike synteser. For å oppnå dette må du ha alle reaksjonene som er beskrevet i emnet tilgjengelig i minnet. Du må huske noen reaksjoner mye oftere enn andre, og den eneste måten å mestre dette målet er å øve på. Eksemplene i dette kapitlet vil være relativt enkle, men du vil snart se at du kan lage noen ganske sofistikerte synteser ved hjelp av et begrenset antall grunnleggende reaksjoner.
Studiet av organisk kjemi utsetter en student for et bredt spekter av sammenhengende reaksjoner. Alkener kan for eksempel omdannes til strukturelt lignende alkaner, alkoholer, alkylhalogenider, epoksider, glykoler og boraner; spaltet til mindre aldehyder, ketoner og karboksylsyrer, og forstørret ved karbokering og radikale tilsetninger samt syklusbelastninger. Alle disse produktene kan senere transformeres til en rekke nye forbindelser som inneholder et stort utvalg funksjonelle grupper, og derved åpne for ytterligere utdyping. Følgelig blir den logiske oppfatningen av en flertrinnssyntese for konstruksjon av en bestemt forbindelse fra et spesifisert utgangsmateriale et av de mest utfordrende problemene som kan stilles.
En ett eller to trinns sekvens av enkle reaksjoner er ikke så vanskelig å utlede. Hvis man for eksempel blir bedt om å fremstille meso-3,4-heksandiol fra 3-heksyn, innser de fleste studenter at det vil være nødvendig å redusere alkynen til cis eller trans-3-heksen før de utfører glykoldannelse. Permanaganat eller osmiumtetroksydhydroksylering av cis-3-heksen ville danne den ønskede meso-isomer. Fra trans-3-heksen ville det være nødvendig å først epoksidisere alkenen med en persyre, etterfulgt av ringåpning med hydroksidion. Dette eksemplet illustrerer et vanlig trekk ved syntese: ofte er det mer enn én effektiv prosedyre som fører til ønsket produkt.
Lengre flertrinnssynteser krever nøye analyse og tanke, siden mange alternativer må vurderes. Som en ekspert sjakkspiller som vurderer fordeler og ulemper ved potensielle trekk på lang sikt, må kjemikeren vurdere den potensielle suksessen til ulike mulige reaksjonsveier, og fokusere på omfanget og begrensningene som begrenser hver av de individuelle reaksjonene som brukes. Dette kan være en skremmende oppgave, som ferdigheten tilegnes av erfaring, og ofte prøving og feiling.
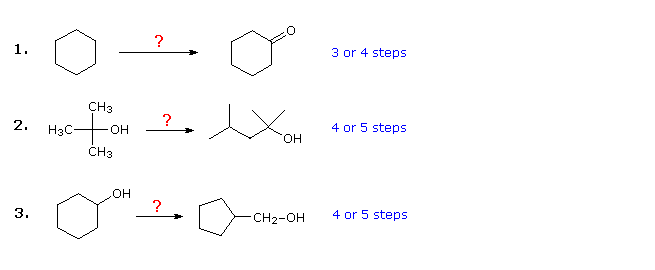
De tre eksemplene vist nedenfor er illustrative. Den første er et enkelt funksjonelt gruppekonverteringsproblem, som i utgangspunktet kan virke vanskelig. Det er ofte nyttig å jobbe slike problemer bakover, med utgangspunkt i produktet. I dette tilfellet bør det være åpenbart at cykloheksanol kan erstattes av cykloheksanon, siden sistnevnte da kan fremstilles ved en enkel oksidasjon. Siden cykloheksan (og alkaner generelt) er relativt ureaktivt, vil bromering (eller klorering) også synes å være et åpenbart første trinn. På dette tidspunktet blir man fristet til å omdanne bromsykloheksan til cykloheksanol ved en SN2-reaksjon med hydroksidion. Denne reaksjonen vil utvilsomt være ledsaget av E2-eliminering, så det ville være renere, selv om det er et trinn lenger, å først lage cykloheksen og deretter hydrere det ved hjelp av en av flere metoder (for eksempel oksymerkning og hydroborering) inkludert den som vises ved å klikke på diagrammet
 Svar
Svar
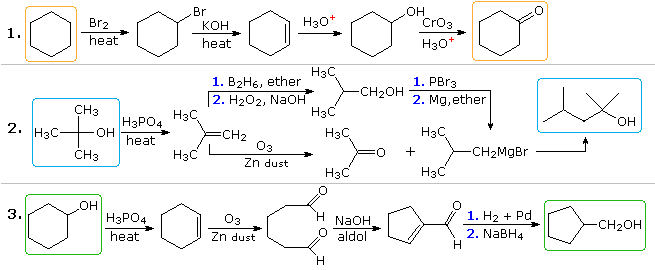
Plausible løsninger for det andre og tredje problemet vises også over På dette punktet. I oppgave 2 har det ønskede produktet syv karbonatomer og utgangsmaterialet har fire. Det er klart at to mellomprodukter avledet fra utgangsforbindelsen må sammenføyes, og ett karbon må gå tapt, enten før eller etter at denne bindingen finner sted. 3º-alkoholfunksjonen i produktet antyder dannelse av et Grignard-tilskudd til et keton, og isobuten ser ut til å være en god forløper for hver av disse reaktantene, som vist. Reaktanten og produktforbindelsene i det tredje problemet er isomerer, men en slags bindingsbrytende og bindingsdannende sekvens er helt klart nødvendig for at denne strukturelle endringen skal skje. En mulig prosedyre er vist ovenfor. Syrekatalysert omorganisering av cykloheksenoksyd, etterfulgt av reduksjon, kan også tjene.
Den nyttige tilnærmingen til å trene synteser som starter fra målmolekylet og arbeide bakover mot enklere utgangsmaterialer er blitt formalisert av professor E. J. Corey (Harvard) og betegnet retrosyntetisk analyse. I denne prosedyren transformeres målmolekylet gradvis til enklere strukturer ved å koble fra utvalgte karbon-karbonbindinger. Disse frakoblingene hviler på transformasjoner, som er det motsatte av plausible syntetiske konstruksjoner. Hver enklere struktur, så generert, blir utgangspunktet for ytterligere frakoblinger, noe som fører til et forgrenet sett med sammenhengende mellomprodukter. En retrosyntetisk transformasjon er avbildet av symbolet = >, som vist nedenfor for tidligere eksempler 2 & 3. Når en fullstendig analyse er utført kan den ønskede syntese utføres ved anvendelse av reaksjonene som ligger til grunn for transformasjonene.
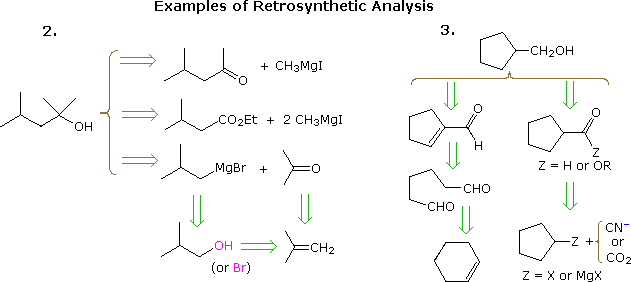
Diagrammet ovenfor gir ikke et komplett sett med transformasjoner for dette målet forbindelser. Når et startmateriale er spesifisert, som i problemene ovenfor, må de foreslåtte banene gjenspeile den begrensningen. Således passer ikke 4-metyl-2-pentanon og 3-metylbutyratester i eksempel 2, selv om de er helt rimelige, ikke med en tert-butanol-start. Likeledes kan et cyklopentyl-mellomprodukt gi en utmerket rute til produktet i eksempel 3, men oppfyller ikke de spesifiserte betingelser for problemet. Hvis den gjennomføres uten skjevhet, vises det noen ganger uvanlige og spennende muligheter. Dessverre fører molekylær kompleksitet (sammensatt av størrelse, funksjonalitet, innblanding av heteroatom, syklisk tilkobling og stereoisomerisme) generelt til veldig store og omfattende forgrenede transformasjonstrær. Datastøttet analyse har vist seg nyttig, men til slutt spiller instinktene og erfaringene til kjemikeren en avgjørende rolle for å komme fram til en vellykket syntetisk plan. Noen relativt enkle eksempler, de fleste med begrensninger i utgangsmaterialet, er gitt nedenfor.
Øvelser
Spørsmål
Q9.9.1
Starter ved 3-heksyn forutsier syntetiske veier for å oppnå:
A – cis-3-heksen
B – 3,4-dibromheksan
C – 3-heksanol
Q9.9.2
Startende med acetylen og eventuelle alkylhalogenider foreslår en syntese for å lage (a) pentanal og (b) heksan.
Løsninger
S9.9.1

S9.9.2
.png?revision=1)
Bidragsytere og attribusjoner
-
Dr. Dietmar Kennepohl FCIC (professor i kjemi, Athabasca University)
-
Prof. Steven Farmer (Sonoma State University)
-
William Reusch, professor emeritus (Michigan State U.), virtuell lærebok for organisk kjemi