Umgestaltete CAR-T-Zelltherapie reduziert Nebenwirkungen in der ersten klinischen Studie
20. Februar 2020, von NCI-Mitarbeitern
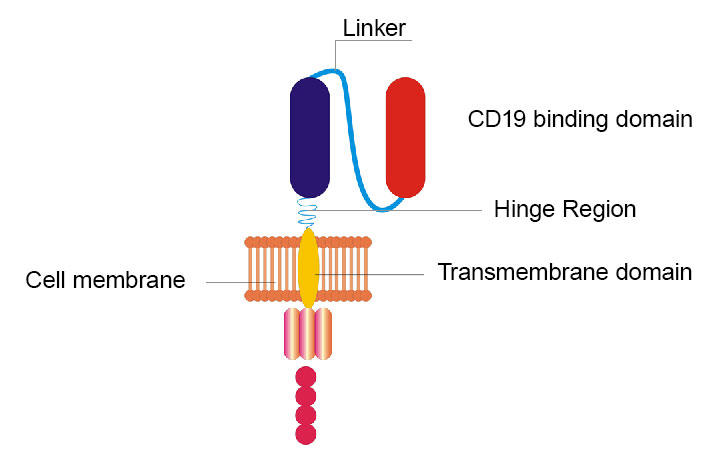
NCI-Forscher haben ihr ursprüngliches CD19-CAR durch Ersetzen des Scharniers und umgebaut Transmembrandomänen und Austausch der CD19-Bindungsdomäne von einem in Mäusen gefundenen Proteinfragment gegen ein ähnliches Fragment beim Menschen.
Im Laufe mehrerer Jahrzehnte haben NCI-Wissenschaftler umfangreiche Grundlagen für einen Roman gelegt Behandlung, die schließlich zu Axicabtagene Ciloleucel (Yescarta) werden würde, einer CAR-T-Zelltherapie für Erwachsene mit Lymphom.
Während die Therapie bei einigen Patienten mit sehr fortgeschrittenem Krebs zu lang anhaltenden Remissionen führen kann, kann sie auch neurologische Nebenwirkungen wie Sprachprobleme, Zittern, Delirium und Krampfanfälle verursachen. Einige Nebenwirkungen können schwerwiegend oder tödlich sein.
Im Jahr 2017 haben NCI-Forscher ihr ursprüngliches CAR-T-Zell-Design mit dem Ziel optimiert, eine sicherere und effektivere Therapie zu schaffen. Die Ergebnisse der ersten klinischen Studie mit den umgebauten CAR-T-Zellen deuten darauf hin, dass sie möglicherweise einen Teil ihres Ziels erreicht haben.
Die neue Therapie verursachte weitaus weniger neurologische Nebenwirkungen als die ursprüngliche Therapie in einer früheren Studie. dennoch war es genauso effektiv. Die Ergebnisse wurden am 20. Januar in Nature Medicine veröffentlicht.
„Es ist bemerkenswert, dass von 20 Patienten in dieser Studie nur einer schwerwiegende neurologische Nebenwirkungen hatte“, sagte Jennifer Brudno, Associate Investigator des NCI Center for Krebsforschung.
„Dies scheint ein bedeutender Fortschritt in unserem derzeitigen Verständnis der Funktionsweise von CAR T-Zellen und der Herstellung eines sichereren CAR T zu sein“, sagte Dr. David Maloney, Ph.D., Medical Direktor der zellulären Immuntherapie des Fred Hutchinson Cancer Research Center, der nicht an der Studie beteiligt war.
Die Studie ist jedoch durch die geringe Anzahl der betroffenen Patienten und die relativ kurze Zeitspanne, in der die Ergebnisse der Patienten verfolgt wurden, begrenzt, fügte er hinzu.
T-Zellen erhalten ein neues CAR
Bei der CAR-T-Zelltherapie werden die eigenen T-Zellen eines Patienten (eine Art weißer Blutkörperchen) mit einem speziellen Protein namens CAR oder chimär bewaffnet Antigenrezeptor. Dieser Rezeptor hilft den T-Zellen, den Krebs der Person zu finden und abzutöten.
Das umgebaute CAR des NCI-Teams unterscheidet sich in einigen Punkten vom Original. Zum Beispiel wurden zwei Abschnitte (als Gelenk- und Transmembrandomänen bezeichnet) des ursprünglichen CAR ersetzt. Ein anderer Abschnitt, der ursprünglich aus einem in Mäusen gefundenen Proteinfragment bestand, wurde gegen ein ähnliches Fragment ausgetauscht, das in Menschen gefunden wurde. Wie das Original zielt das neue CAR aber auch auf CD19 ab, ein Molekül, das die Oberfläche von Lymphomzellen untersucht.
In früheren Laborstudien stellten die Forscher fest, dass mit dem neuen CAR bewaffnete T-Zellen das Wachstum von Tumoren bei Mäusen verlangsamten. Und im Vergleich zu den ursprünglichen CAR-T-Zellen produzierten die neuen CAR-T-Zellen geringere Mengen an Substanzen, die als Zytokine bezeichnet werden.
Wissenschaftler verstehen nicht vollständig, wie CAR-T-Zellen neurologische Nebenwirkungen verursachen, aber Zytokine können teilweise dazu führen Schuld. Zytokine sind auch der Schuldige für das Zytokinfreisetzungssyndrom, eine weitere potenziell lebensbedrohliche Nebenwirkung der CAR-T-Zelltherapie.
Mit diesen vielversprechenden Ergebnissen führte das Team eine erste Studie am Menschen über die umgebauten CAR-T-Zellen durch.
Weniger Zytokine, weniger neurologische Nebenwirkungen
n der neuen Studie gaben Dr. Brudno und ihre Kollegen 20 Patienten mit B-Zell-Lymphom die neue CAR-T-Zelltherapie.
Insgesamt zeigten vier Patienten (20%) eine gewisse neurologische Toxizität: Drei hatten milde Wirkungen und einer (5%) hatte schwere Wirkungen, die nach der Behandlung mit einem Steroid (Arzneimittel, das das Immunsystem unterdrückt) schnell verschwanden ).
In einer früheren Studie zur ursprünglichen CAR-T-Zelltherapie mit 22 Personen mit B-Zell-Lymphom zeigten 17 (77%) eine gewisse neurologische Toxizität – darunter 11 Patienten (50%) mit schweren Symptomen.
Zwei Patienten (10%) in der neuen Studie und vier (18%) in der früheren Studie hatten ein schweres Zytokinfreisetzungssyndrom. „Es scheint günstig, dass ähnlich, aber es ist schwer zu sagen, ob es definitiv weniger häufig ist“, sagte Dr. Brudno bei der neuen Therapie.
Die Cytokinspiegel im Blut von Patienten, die mit der neuen Therapie behandelt wurden, waren niedriger Als bei Patienten, die die ursprüngliche Therapie erhielten, fanden die Wissenschaftler heraus, was erklären könnte, warum die neue Therapie weniger neurologische Nebenwirkungen verursachte.
In beiden Studien verwendeten die Forscher dieselben Methoden, um den Schweregrad zu bewerten Dr. Brudno bemerkte die neurologische Toxizität und das Zytokinfreisetzungssyndrom.
Und obwohl es andere Ähnlichkeiten zwischen den beiden Studien gibt – sie wurden beispielsweise in derselben Einrichtung durchgeführt -, ist es schwierig, Ergebnisse aus unabhängigen Studien zu vergleichen, sagte sie.
Verbleibende CAR-T-Zellen
Ein Problem bei aktuellen CAR-T-Zelltherapien ist, dass die Zellen im Körper des Patienten nicht sehr lange halten. Dies liegt zum Teil daran, dass das menschliche Immunsystem Mausproteine als unbekannt ansehen und die CAR-T-Zellen zerstören kann.
Teil des Ziels des Teams war es, CAR T-Zellen zu erstellen, die länger bestehen bleiben oder bestehen bleiben. Sie schlussfolgerten, dass T-Zellen mit einem CAR aus allen menschlichen Proteinen möglicherweise länger halten als Zellen mit einem CAR, das Mausproteine enthält.
Wenn das Immunsystem des Patienten ein aus menschlichen Proteinen hergestelltes CAR ignoriert, halten die CAR-T-Zellen möglicherweise länger und sind effektiver, erklärte Dr. Brudno.
Dies kann der Fall sein für die neue Therapie. Einen Monat nach Erhalt der Behandlung gab es im Blut von Patienten, die die neue Therapie erhielten, höhere Spiegel an CAR-T-Zellen als bei Patienten, die mit der ursprünglichen Therapie behandelt wurden.
Diese Ergebnisse sind „ermutigend“ und sollten es sein In zukünftigen Studien untersucht, sagte Dr. Maloney.
Obwohl die neuen CAR-T-Zellen länger zu bestehen scheinen als die ursprünglichen CAR-T-Zellen, schienen sie nicht wirksamer zu sein. In beiden Studien mehr als die Hälfte (55%) der Teilnehmer gingen in eine vollständige Remission.
Es ist jedoch „ermutigend“, „zusätzlich zu der geringen Toxizität“ eine sehr gute Wirksamkeit für dieses CAR-T-Zell-Produkt zu sehen „, so Dr. Brudno sagte.
Eine informative Neugestaltung
CAR-T-Zelltherapie kann zu einer Vielzahl von neurologischen Effekten führen, die von sehr mild bis schwer und lebensbedrohlich reichen, erklärte Dr. Brudno.
Diese Nebenwirkungen sind mit allen derzeit verfügbaren CAR-T-Zelltherapien verbunden – zwei von der FDA zugelassene und eine weitere ausstehende FDA-Zulassung -, stellte Dr. Maloney fest udies lagen die Raten schwerer neurologischer Toxizität zwischen 5% und 50%.
Andere klinische Studien testen CAR-T-Zelltherapien, die ebenfalls neu gestaltet wurden, um sicherer zu sein, bemerkte Dr. Maloney. Die neue NCI-Studie identifiziert Aspekte des CAR-T-Zell-Designs, von denen bisher nicht bekannt war, dass sie die neurologische Toxizität beeinflussen, sagte er.
„Aber wie Sie das in ein neues kommerzielles Produkt übersetzen oder ein kommerzielles Produkt aufrüsten, ist eine ganz andere Frage“, sagte er. Die Herstellung einer CAR-T-Zelltherapie für jeden einzelnen Patienten ist ein komplexer und teurer Prozess kann nur in hochspezialisierten Einrichtungen durchgeführt werden.
Derzeit konzentriert sich das NCI-Team unter der Leitung von James Kochenderfer, MD, auf die Durchführung klinischer Studien mit verschiedenen CAR-T-Zelltherapien für Menschen mit einer anderen Blutgruppe Krebs, Multiples Myelom.