Ombyggd C-T-cellterapi minskar biverkningar i första kliniska prövningen
20 februari 2020, av NCI-personal
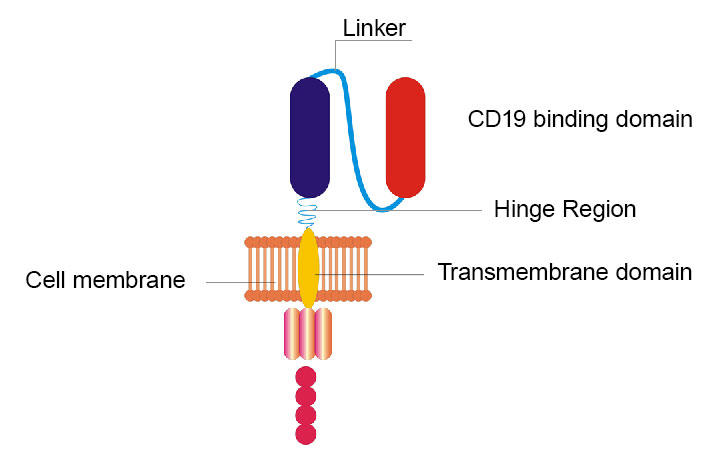
NCI-forskare gjorde om sin ursprungliga CD19 CAR genom att byta ut gångjärnet och transmembrandomäner och byta CD19-bindande domän från ett proteinfragment som finns i möss till ett liknande fragment som finns hos människor.
Under flera decennier lade NCI-forskare omfattande grund för en roman behandling som så småningom skulle bli Axicabtagene ciloleucel (Yescarta), en CAR T-cellterapi för vuxna med lymfom.
Även om behandlingen kan leda till långvariga remissioner för vissa patienter med mycket avancerad cancer, kan den också orsaka neurologiska biverkningar som talproblem, tremor, delirium och anfall. Vissa biverkningar kan vara allvarliga eller dödliga.
Så, 2017, NCI forskare justerade sin ursprungliga CAR T-cell design med målet att skapa en säkrare och effektivare behandling. Nu tyder resultaten från den första kliniska prövningen av de ombyggda CAR T-cellerna på att de kan ha uppnått en del av sitt mål.
Den nya behandlingen orsakade mycket färre neurologiska biverkningar än den ursprungliga behandlingen gjorde i en tidigare studie, ändå var det lika effektivt. Resultaten rapporterades den 20 januari i Nature Medicine.
”Det är anmärkningsvärt att av 20 patienter i den här studien, var det bara en som hade allvarliga neurologiska biverkningar”, säger biträdande utredare Jennifer Brudno, MD, vid NCIs Center for Cancerforskning.
”Detta verkar vara ett betydande framsteg i vår nuvarande förståelse för hur CAR T-celler fungerar och hur man gör en säkrare CAR T,” säger David Maloney, MD, doktor, medicinsk chef för cellulär immunterapi för Fred Hutchinson Cancer Research Center, som inte var inblandad i studien.
Studien är dock begränsad av det lilla antalet inblandade patienter och den relativt korta tiden patienternas resultat har spårats, tillade han.
T-celler får en ny CAR
CAR-T-cellterapi innebär att en patients egna T-celler (en typ av vita blodkroppar) beväpnas med ett specialiserat protein som kallas CAR eller chimer antigenreceptor. Denna receptor hjälper T-cellerna att hitta och döda personens cancer.
NCI-teamets ombyggda CAR skiljer sig från originalet på några sätt. Till exempel ersattes två sektioner (kallade gångjärn och transmembrandomäner) i den ursprungliga CAR. Och ett annat avsnitt som ursprungligen bestod av ett proteinfragment som hittades hos möss byttes mot ett liknande fragment som hittades hos människor. Men, precis som originalet, riktar den nya bilen också CD19, en molekyl som tappar ytan på lymfomceller.
I tidigare laboratoriestudier fann forskarna att T-celler beväpnade med den nya CAR bromsade tillväxten av tumörer hos möss. Och jämfört med de ursprungliga CAR T-cellerna producerade de nya CAR T-cellerna lägre nivåer av ämnen som kallas cytokiner.
Forskare förstår inte helt hur CAR T-celler orsakar neurologiska biverkningar, men cytokiner kan delvis vara skylla. Cytokiner är också gärningsmannen för cytokinfrisättningssyndrom, en annan potentiellt livshotande biverkning av CAR T-cellterapi.
Med dessa lovande resultat gick laget framåt med en första in-human-studie av de ombyggda CAR-T-cellerna.
Färre cytokiner, färre neurologiska biverkningar
I den nya prövningen gav Dr Brudno och hennes kollegor den nya CAR-T-cellterapin till 20 patienter med B-celllymfom.
Sammantaget upplevde fyra patienter (20%) viss neurologisk toxicitet: Tre hade milda effekter och en (5%) upplevde allvarliga effekter som snabbt försvann efter behandling med en steroid (läkemedel som försämrar immunförsvaret ).
I en tidigare studie av den ursprungliga CAR T-cellterapin som involverade 22 personer med B-celllymfom upplevde 17 (77%) viss neurologisk toxicitet – inklusive 11 patienter (50%) som upplevde svåra symtom.
Två patienter (10%) i den nya studien och fyra (18%) i den tidigare studien hade svårt cytokinfrisättningssyndrom. ”Det verkar gynnsamt att liknande, men det är svårt att säga om det är definitivt mindre frekvent” med den nya behandlingen, säger Dr. Brudno.
Cytokinnivåerna var lägre i blodet hos patienter som behandlades med den nya behandlingen. än hos patienter som fick den ursprungliga behandlingen, fann forskarna, vilket kan förklara varför den nya behandlingen orsakade färre neurologiska biverkningar, skrev de.
I båda studierna använde forskarna samma metoder för att klassificera svårighetsgraden. av neurologisk toxicitet och cytokinfrisättningssyndrom, konstaterade Dr Brudno.
Och även om det finns andra likheter mellan de två försöken – de genomfördes till exempel på samma anläggning – är det svårt att jämföra resultat från oberoende studier, sa hon.
CAR T-celler som håller fast
Ett problem med nuvarande CAR T-cellterapier är att cellerna inte håller så länge i patientens kropp. Det beror delvis på att det mänskliga immunsystemet kan se musproteiner som okända och förstöra CAR T-cellerna.
En del av lagets mål var att skapa CAR T-celler som håller sig kvar, eller kvarstår längre. De resonerade att T-celler med en CAR gjord av alla humana proteiner kan vara längre än celler med en CAR som innehåller musproteiner.
Om patientens immunsystem ignorerar en BIL gjord av humana proteiner, kan CAR T-cellerna vara längre och vara mer effektiva, förklarade Dr. Brudno.
Det kan vara fallet för den nya behandlingen. En månad efter att ha fått behandlingen fanns det högre nivåer av CAR T-celler i blodet hos patienter som fick den nya behandlingen än hos de som behandlades med den ursprungliga behandlingen.
Dessa resultat är ”uppmuntrande” och bör vara undersöktes i framtida studier, säger Dr. Maloney.
Även om de nya CAR-T-cellerna verkar bestå längre än de ursprungliga CAR-T-cellerna verkade de inte vara mer effektiva. I båda försöken, mer än hälften (55%) av deltagarna gick i fullständig eftergift.
Men det är ”uppmuntrande” att se ”mycket bra effekt för denna CAR-T-cellprodukt, förutom den låga toxiciteten”, säger Dr. Brudno sade.
En informativ nydesign
T-cellterapi för bil kan leda till ett varierat utbud av neurologiska effekter, allt från mycket mild till svår och livshotande, förklarade Dr. Brudno.
Dessa biverkningar är associerade med alla tillgängliga CAR-T-cellterapier – två som är FDA-godkända och en annan i väntan på FDA-godkännande – konstaterade Dr Maloney. udies har frekvensen av allvarlig neurologisk toxicitet varierat från 5% till 50%.
Andra kliniska prövningar testar CAR T-cellterapier som också har redesignats för att vara säkrare, konstaterade Dr Maloney. Den nya NCI-studien identifierar aspekter av CAR T-celldesign som inte tidigare var kända för att påverka neurologisk toxicitet, sa han.
”Men hur du översätter det till en ny kommersiell produkt eller uppgraderar kommersiell produkt är en helt annan fråga”, sa han. Att tillverka en CAR-T-cellterapi för varje enskild patient är en komplex och dyr process som kan bara göras på högt specialiserade anläggningar.
För närvarande är NCI-teamet, ledt av James Kochenderfer, MD, fokuserat på att genomföra kliniska prövningar av olika CAR T-cellterapier för personer med en annan typ av blod cancer, multipelt myelom.