De draagbare cardioverter-defibrillator: een leven (vest) van controverse

De VS De Food and Drug Administration (FDA) keurde in 2001 een medisch hulpmiddel goed nadat de cruciale klinische proef de veiligheid en werkzaamheid had aangetoond bij vijf van de zeven patiënten die werden behandeld.1 Al meer dan tien jaar variëren real-world observationele studies met het beschreven medische apparaat. interpretaties van bruikbaarheid.
In 2018, 17 jaar na goedkeuring door de FDA, lieten de resultaten van de eerste gerandomiseerde gecontroleerde studie van het medische hulpmiddel negatieve resultaten zien.2 Tot op de dag van vandaag wordt dit medische hulpmiddel nog steeds voorgeschreven, en is in bepaalde instellingen de standaard van zorg geworden. Dit is het verhaal van de LifeVest®, de enige door de FDA goedgekeurde draagbare cardioverter defibrillator (WCD) die is geïndiceerd om het risico op plotselinge hartdood (SCD) te verminderen bij patiënten met een verminderde linkerventrikelejectiefractie (LVEF) die een acuut myocardinfarct hebben gehad (AMI).
De rol van een ICD in de onmiddellijke post-AMI-setting bij patiënten met een LVEF ≤35-40% is eerder onderzocht in twee gerandomiseerde gecontroleerde onderzoeken (DINAMIT en IRIS) .3, 4 In DINAMIT was er een significant lager percentage SCD bij patiënten gerandomiseerd naar ICD dan bij geen ICD (4% vs. 8%; p = 0,009), maar er was een significant hoger percentage niet-SCD sterfgevallen in de ICD-groep dan bij in de groep zonder ICD (15% vs. 9%; p = 0,02). Evenzo was er bij IRIS een significant lager percentage SCD bij patiënten gerandomiseerd naar ICD dan bij geen ICD (6% vs. 13%; p = 0,049), maar er was een significant hoger percentage niet-SCD sterfgevallen in de ICD-groep dan bij in de groep zonder ICD (15% vs. 9%; p = 0,001).
Hoewel ICDs in deze gerandomiseerde onderzoeken werden geassocieerd met een lager risico op SCZ, werd dit gecompenseerd door de associatie met een hoog risico van niet-SCD-evenementen. Als gevolg hiervan bevelen de huidige richtlijnen van de ACC / AHA / HRS ICD-implantatie aan voor primaire preventie van SCD bij deze populatie na een periode van 40 dagen van richtlijngerichte medische therapie (of een periode van 90 dagen van richtlijngerichte medische therapie als revascularisatie uitgevoerd) (Figuur 1) .5
Figuur 1: Primaire preventie van SCZ bij patiënten met ischemische hartziekte
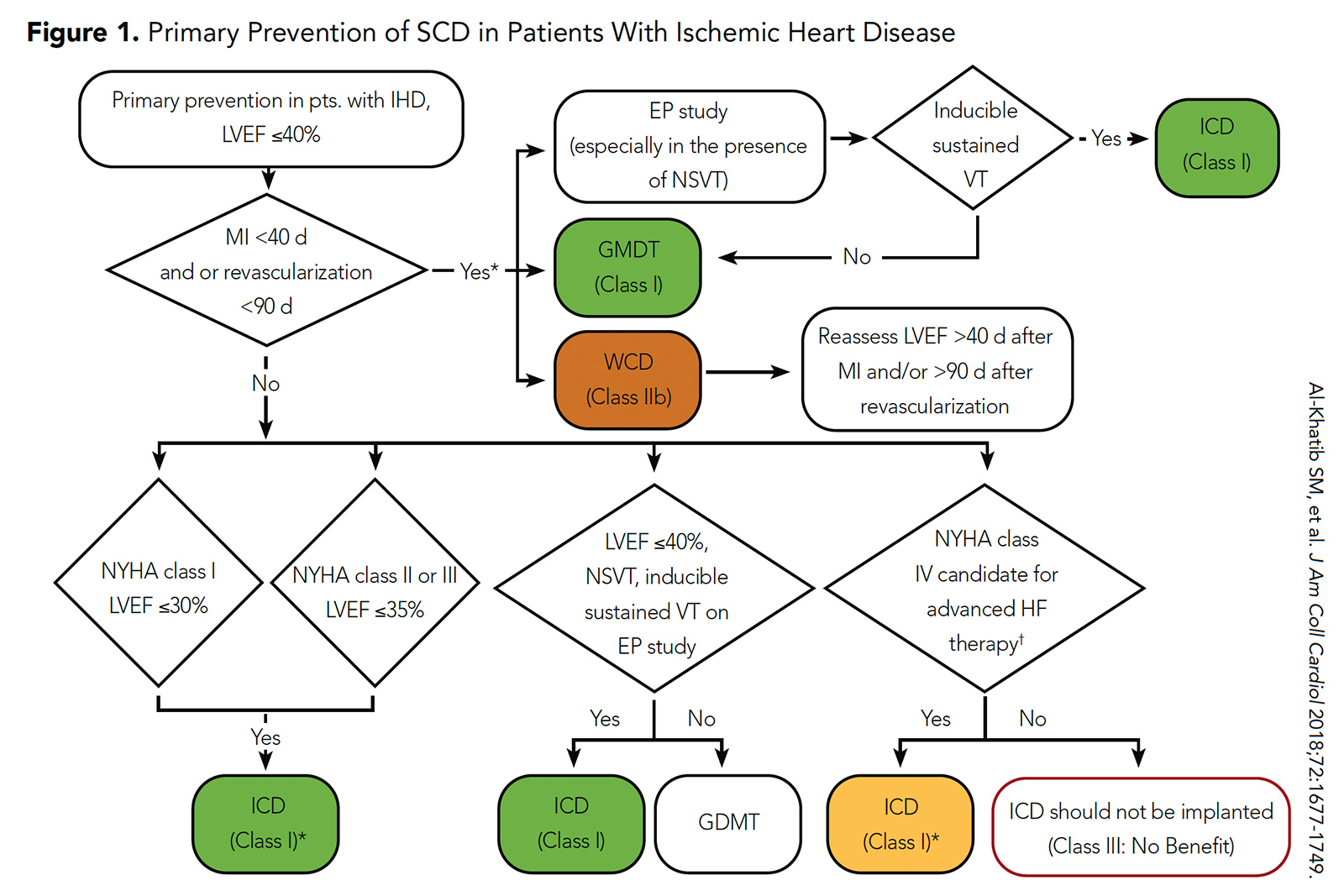 Klik op de afbeelding hierboven voor een grotere weergave.
Klik op de afbeelding hierboven voor een grotere weergave. Figuur 2: ACC / AHA / HRS-richtlijn 2017 voor gebruik van draagbare cardioverter-defibrillatoren
 Klik op de afbeelding hierboven voor een grotere weergave.
Klik op de afbeelding hierboven voor een grotere weergave.
Het risico op SCZ in de periode onmiddellijk na AMI is echter het hoogst in de eerste 30 dagen. Aan het VALIANT-onderzoek namen 14.609 patiënten deel met een LVEF ≤40% na AMI en toonde aan dat 7% van de patiënten een plotselinge dood of hartstilstand ervoer gedurende een follow-upperiode van twee jaar. Een alarmerende 19% van deze sterfgevallen vond plaats in de eerste 30 dagen na AMI, en het risico was het hoogst bij patiënten met een LVEF ≤ 30% (2,3% per maand) .6
Samengenomen met de resultaten van DINAMIT en IRIS, wezen de resultaten van VALIANT op de noodzaak van een niet-ICD-strategie om patiënten te beschermen tegen het optreden van SCZ. De WCD, die al door de FDA was goedgekeurd ten tijde van deze onderzoeken, bleek de perfecte oplossing.
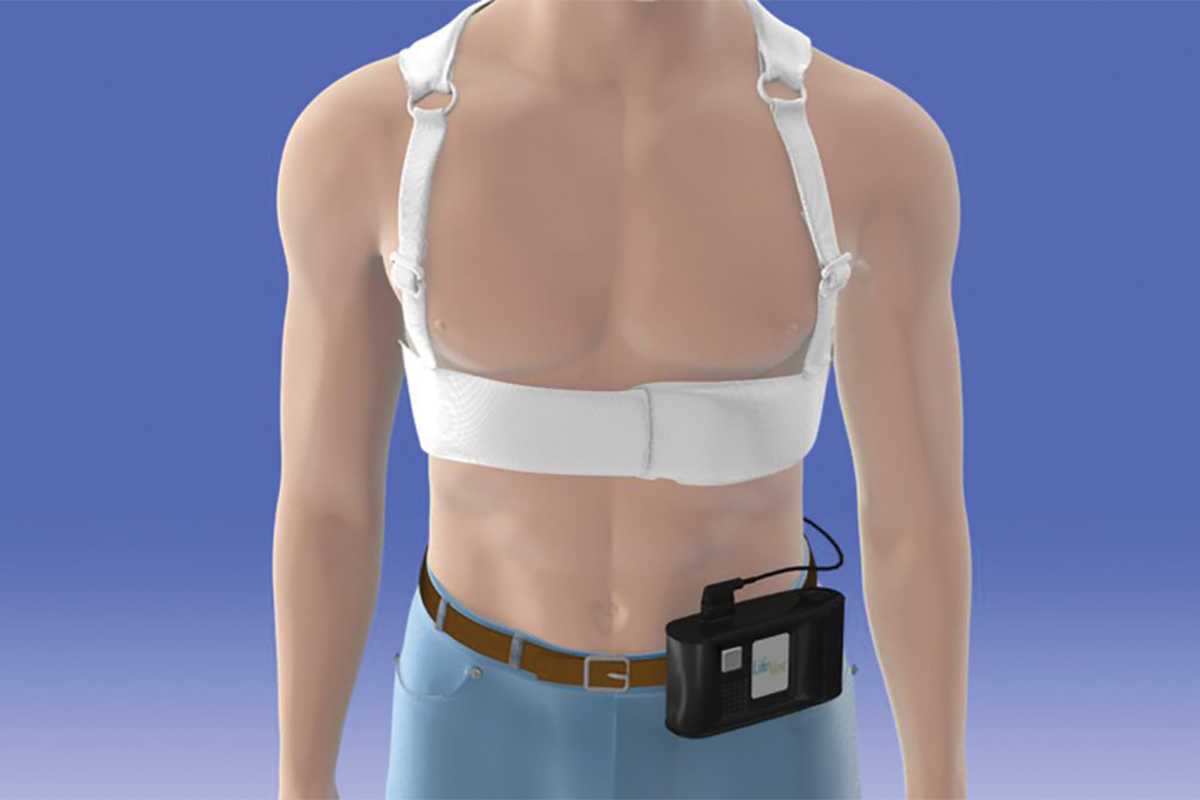
De momenteel beschikbare versie van de WCD is het LifeVest van Zoll Medical Corporation.7 Het apparaat bestaat uit een borstkas met twee defibrillator-elektroden die verticaal langs de rug zijn geplaatst, een frontale riem met een horizontaal gepositioneerde defibrillator-elektrode met elektroden die het hartritme detecteren, en een kleine monitorbox die de ritmes registreert en de batterij bevat. Eenmaal geactiveerd, kan het LifeVest de patiënt drie mogelijke alarmen geven: een gongalarm dat aangeeft dat aandacht nodig is voor de monitorbox; een trilalarm dat aangeeft dat een dodelijke aritmie is gedetecteerd en dat de WCD-behandelingssequentie wordt geactiveerd; en een sirenewaarschuwing die aangeeft dat er een schok op handen is. Direct voordat de schok wordt toegediend, wordt een blauwe gel van de drie defibrillatie-elektroden op de patiënt losgelaten om het contact voor elektrische geleiding te verbeteren. De schokvector bevindt zich tussen de defibrillatorpads op de rug en het defibrillatorkussen in de voorste gordel.
De praktijkervaring met de WCD is beschreven in talrijke onderzoeken die zijn gepubliceerd van 2001 tot 2018. Een van de De grootste bestudeerde patiëntencohorten omvatten 8.453 patiënten uit het Zoll-register. In totaal kregen 133 patiënten (1,6%) 309 geschikte schokken, waarbij 91% van de schokken met succes de patiënt reanimeerde na een ventriculaire tachyaritmie (84% bij niet-revascularisatiepatiënten en 95% bij gerevasculariseerde patiënten). De mediane tijd van AMI tot shock was 16 dagen, en 75% van de schokken trad op in de maand na AMI.8
De langverwachte VEST-studie werd door de hoofdauteur gepresenteerd als een laattijdige klinische studie Jeffrey E. Olgin, MD, FACC, bij ACC.18, en uiteindelijk gepubliceerd in de New England Journal of Medicine.Het doel van de VEST-studie was om de werkzaamheid van de WCD te bepalen in de periode voordat ICDs worden geïndiceerd bij patiënten met een MI en een verminderde LVEF. Gedurende een inschrijvingsperiode van bijna tien jaar werden in het onderzoek 2.302 patiënten met AMI en een LVEF ≤35% gerandomiseerd in een verhouding van 2: 1 ten opzichte van WCD versus geen WCD. De analyse werd uitgevoerd op een intent-to-treat-manier.
De resultaten van VEST waren opmerkelijk omdat er geen significant verschil was in de primaire samengestelde uitkomst van plotseling overlijden of overlijden door ventriculaire tachycardie of ventrikelfibrilleren na 90 dagen (aritmisch overlijden), die optraden bij 1,6% van de patiënten in de WCD-groep en bij 2,4% van de patiënten in de niet-WCD-groep (relatief risico 0,66; 95% betrouwbaarheidsinterval 0,37-121; p = 0,18).
Met name 43 patiënten (2,8%) in de WCD-groep droegen nooit een apparaat en 20 patiënten (2,6%) in de niet-WCD-groep kregen het apparaat buiten de studie om; 10 patiënten in de WCD-groep (0,7%) en 15 patiënten in de niet-WCD-groep (1,5%) gingen verloren voor follow-up, en twee patiënten in elke groep (5% totaal) hadden onvoldoende gegevens om de oorzaak van plotselinge dood. De auteurs uitten hun bezorgdheid dat het niet naleven van het dragen van de WCD in de WCD-groep de kracht van het onderzoek kan hebben verminderd, aangezien de verwachte draagtijd van de WCD van 70% pas in de eerste twee weken van de proef werd gehaald. Uiteindelijk werd de VEST-studie gezien als een negatieve studie voor het vermogen van de WCD om het risico op SCZ in zijn doelgroep significant te verminderen.2
De negatieve resultaten leken echter het gebruik van WCD niet te ontmoedigen en moedigde in plaats daarvan onderzoekers aan om zijn bevindingen aan te vechten. De grootste beschikbare meta-analyse van 28 onderzoeken met 33.242 patiënten (inclusief de interventionele arm van de VEST-studie) van 2001-2018 onthulde dat geschikte WCD-behandelingen, geschikte WCD-schokken en ongepaste WCD-schokken optraden bij 7/100-personen , Respectievelijk 5/100-personen en 2/100-personen, gedurende een periode van drie maanden.
In deze meta-analyse ondervonden patiënten met ischemische cardiomyopathie, niet-ischemische cardiomyopathie en gemengde cardiomyopathie passende WCD behandelingen met een snelheid van respectievelijk 8/100-personen, 6/100-personen en 3/100-personen, gedurende een periode van drie maanden. Vergeleken met patiënten met ischemische cardiomyopathie in VEST, vertoonden patiënten met ischemische cardiomyopathie in het niet-VEST-cohort een hogere incidentie van geschikte WCD-therapie (11/100-personen versus 1/100-personen gedurende drie maanden). Bij het onderzoeken van het patroon van WCD-voorschrift, maakten de auteurs de interessante observatie dat het voortdurende gebruik van WCD “waarschijnlijk wordt gedreven door de finaliteit van SCD en gedeeltelijk door angst voor rechtszaken, ondanks het ontbreken van gegevens om dit te ondersteunen.” 9
De tweede van deze onderzoeken onderzochten de mortaliteit en kosten die verband houden met WCD-gebruik bij 16.935 patiënten op basis van gegevens van Medicare-claims. Het gebruik van WCD was geassocieerd met een significante vermindering van de mortaliteit na een jaar na AMI (19,8% vs. 11,5%; p = 0,017), en deze 8,3% vermindering van de absolute mortaliteit kwam overeen met een incrementele kosteneffectiviteitsratio (ICER) van $ 12.373,11 Met andere woorden, het gebruik van de WCD kost $ 12.373 om een leven te redden in het eerste jaar na AMI. Volgens de ACC / AHA Statement on Cost / Value Methodology in Clinical Practice Guidelines and Performance Measures, zou de ICER voor de WCD worden geclassificeerd als een waardevolle hulpbron (ICER 12
Hoewel de reis voor WCD-acceptatie omslachtig was, heeft het zijn plaats verdiend op de shortlist van moderne, levensreddende medische hulpmiddelen. Dienovereenkomstig is in de meest recente ACC / AHA / HRS-richtlijn van 2017 het gebruik van een WCD na AMI bij patiënten met een LVEF ≤35% heeft een IIb-aanbeveling gekregen (Figuur 2) .5
Zoals alle therapieën, is de WCD het meest effectief wanneer deze wordt gebruikt zoals voorgeschreven, maar dit vereist een continue naleving tot 90 dagen en constante aandacht voor de verschillende apparaatalarmen die op elk moment kunnen worden geactiveerd. Er zijn ontwikkelingen gaande om de kleding, monitoren en de algehele patiëntervaring te verbeteren, maar naleving zal waarschijnlijk de patiëntenpopulatie beperken die daadwerkelijk baat zal hebben bij dit omslachtige apparaat. In de tussentijd zal het blijven bestaan t o de cardioloog om te beslissen welke patiënten de meest geschikte kandidaten zijn om niet alleen het LifeVest te ontvangen, maar het ook te dragen.

Dit artikel is geschreven door Edward Chu, MD, (@Ed_Chu_MD), elektrofysiologie fellow in training (FIT) in het Mount Sinai Medical Center in New York.
- Feldman AM, Klein H, Tchou P, et al. WEARIT-onderzoekers en coördinatoren; BIROAD-onderzoekers en coördinatoren. Gebruik van een draagbare defibrillator bij het beëindigen van tachyaritmieën bij patiënten met een hoog risico op plotseling overlijden: resultaten van de WEARIT / BIROAD. Pacing Clin Electrophysiol 2004; 27 (1): 4-9.
- Olgin JE, Pletcher MJ, Vittinghoff E, et al. VEST-onderzoekers. Wearable cardioverter-defibrillator na een hartinfarct.N Engl J Med 2018; 379: 1205-15.
- Hohnloser SH, Kuck KH, Dorian P, et al; DINAMIT-onderzoekers. Profylactisch gebruik van een implanteerbare cardioverter-defibrillator na een acuut myocardinfarct. N Engl J Med 2004; 351: 2481-8.
- Steinbeck G, Andresen D, Seidl K, et al; IRIS-onderzoekers. Implantatie van de defibrillator kort na een hartinfarct. N Engl J Med 2009; 361: 1427-36.
- Al-Khatib SM, Stevenson WG, Ackerman MJ, et al. AHA / ACC / HRS-richtlijn 2017 voor de behandeling van patiënten met ventriculaire aritmieën en de preventie van plotselinge hartdood: Samenvatting: een rapport van de American College of Cardiology / American Heart Association Task Force on Clinical Practice Guidelines en de Heart Rhythm Society. J Am Coll Cardiol 2018; 72: 1677-1749.
- Solomon SD, Zelenkofske S, McMurray JJ, et al. Valsartan in onderzoek naar acuut myocardinfarct (VALIANT). Plotselinge dood bij patiënten met een hartinfarct en linkerventrikeldisfunctie, hartfalen of beide. N Engl J Med 2005; 352: 2581-8.
- Zoll LifeVest. Zoll Medical Corporation. Hier beschikbaar Toegang tot 13 september 2020.
- Epstein AE, Abraham WT, Bianco NR, et al. Gebruik van draagbare cardioverter-defibrillatoren bij patiënten die geacht worden een hoog risico te lopen op een vroeg post-myocardinfarct. J Am Coll Cardiol 2013; 62: 2000-7.
- Masri A, Altibi AM, Erqou S, et al. Draagbare cardioverter-defibrillatortherapie ter voorkoming van plotselinge hartdood: een systematische review en meta-analyse. JACC Clin Electrophysiol 2019; 5: 152-61.
- Olgin JE, Lee BK, Vittinghoff E, et al. Gevolgen van compliance van draagbare cardioverter-defibrillatoren op de resultaten in de VEST-studie: as-behandelde en per-protocolanalyses. J Cardiovasc Electrophysiol 2020; 31: 1009-18.
- Clark MA, Szymkiewicz SJ, Volosin K. Sterfte en kosten in verband met draagbare cardioverter-defibrillatoren na een acuut myocardinfarct: een retrospectieve cohortanalyse van medicare-claimgegevens. J Innov Card Rhythm Manag 2019; 10: 3866-73.
- Anderson JL, Heidenreich PA, Barnett PG, et al; ACC / AHA-taskforce voor prestatiemaatstaven; ACC / AHA Task Force voor praktijkrichtlijnen. ACC / AHA-verklaring over kosten / waarde-methodologie in klinische praktijkrichtlijnen en prestatiemaatstaven: een rapport van de American College of Cardiology / American Heart Association Task Force on Performance Measures en Task Force on Practice Guidelines. J Am Coll Cardiol 2014; 63: 2304-22.
Klinische onderwerpen: Aritmieën en klinische EP, SCD / ventriculaire aritmieën
Sleutelwoorden: ACC-publicaties, Cardiology Magazine, Amerikaanse Food and Drug Administration, Apparaatgoedkeuring, Ventrikelfibrillatie, Incidentie, Slagvolume, Risico, Betrouwbaarheidsintervallen, Medicijnen, Kosten -Voordelenanalyse, trillingen, vervolgonderzoeken, doelen, analyse van intentie om te behandelen, verloren voor follow-up, standaardzorg
< Terug naar vermeldingen