ウェアラブルカーディオバーター除細動器:論争の生命(ベスト)

米国2001年に食品医薬品局(FDA)は、その重要な臨床試験が治療を受けた7人の患者のうち5人で安全性と有効性を示した後、医療機器を承認しました。110年以上にわたって、医療機器を使用した実際の観察研究はさまざまであると説明されています。有用性の解釈。
FDAの承認から17年後の2018年、医療機器の最初のランダム化された対照試験の結果は否定的な結果を示しました。2今日まで、この医療機器は処方され続けており、 、特定の施設では、ケアの標準となっています。これは、急性心筋梗塞を患った左心室駆出率(LVEF)が低下した患者の心臓突然死(SCD)のリスクを低減することが示されている、FDAが承認した唯一の装着型除細動器(WCD)であるLifeVest®のストーリーです。 (AMI)。
LVEFが35〜40%以下の患者のAMI直後の設定におけるICDの役割は、2つのランダム化対照試験(DINAMITおよびIRIS)で以前に調査されています。3、 4 DINAMITでは、ICDにランダム化された患者のSCD率はICDなしよりも有意に低かった(4%対8%; p = 0.009)が、ICDグループの非SCD死亡率はICD群よりも有意に高かった。 ICDなしグループ(15%対9%; p = 0.02)。同様に、IRISでは、ICDにランダム化された患者のSCDの割合はICDがない場合よりも有意に低かった(6%対13%; p = 0.049)が、ICDグループの非SCD死亡の割合はICDよりも有意に高かった。 ICDなしのグループ(15%対9%; p = 0.001)。
これらのランダム化試験ではICDはSCDのリスクが低いと関連していたが、これはリスクが高いとの関連によって相殺された。非SCDイベントの。その結果、ACC / AHA / HRSの現在のガイドラインでは、40日間のガイドラインに基づく治療(または血管再生が血管再生の場合は90日間のガイドラインに基づく治療)の後に、この集団におけるSCDの一次予防のためにICD移植を推奨しています。実施)(図1).5
図1:虚血性心疾患患者におけるSCDの一次予防
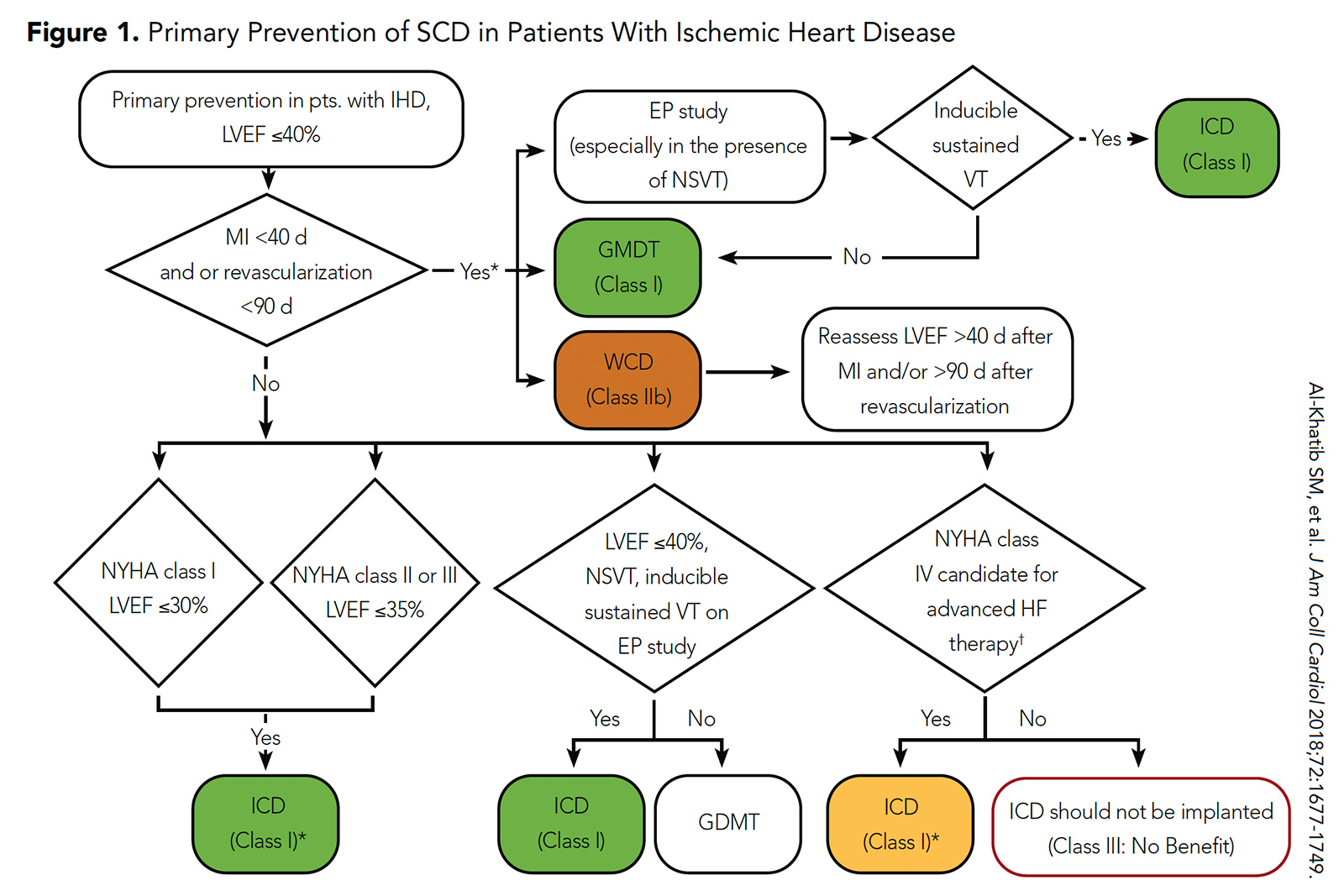 上の画像をクリックすると、拡大表示されます。
上の画像をクリックすると、拡大表示されます。 図2:ウェアラブルカーディオバーター除細動器の使用に関する2017 ACC / AHA / HRSガイドライン
 上の画像をクリックすると、拡大表示されます。
上の画像をクリックすると、拡大表示されます。
ただし、AMI直後のSCDのリスクは、最初の30日間で最も高くなります。 VALIANT試験では、AMI後にLVEFが40%以下の14,609人の患者が登録され、患者の7%が2年間の追跡期間にわたって突然死または心停止を経験したことが示されました。これらの死亡の驚くべき19%はAMI後の最初の30日間に発生し、リスクはLVEFが30%以下の患者で最も高かった(1か月あたり2.3%)6
の結果と合わせてDINAMITとIRIS、VALIANTの結果は、SCDの発生から患者を保護するための非ICD戦略の必要性を示しました。これらの試験の時点ですでにFDAに承認されていたWCDは、完璧なソリューションのようでした。
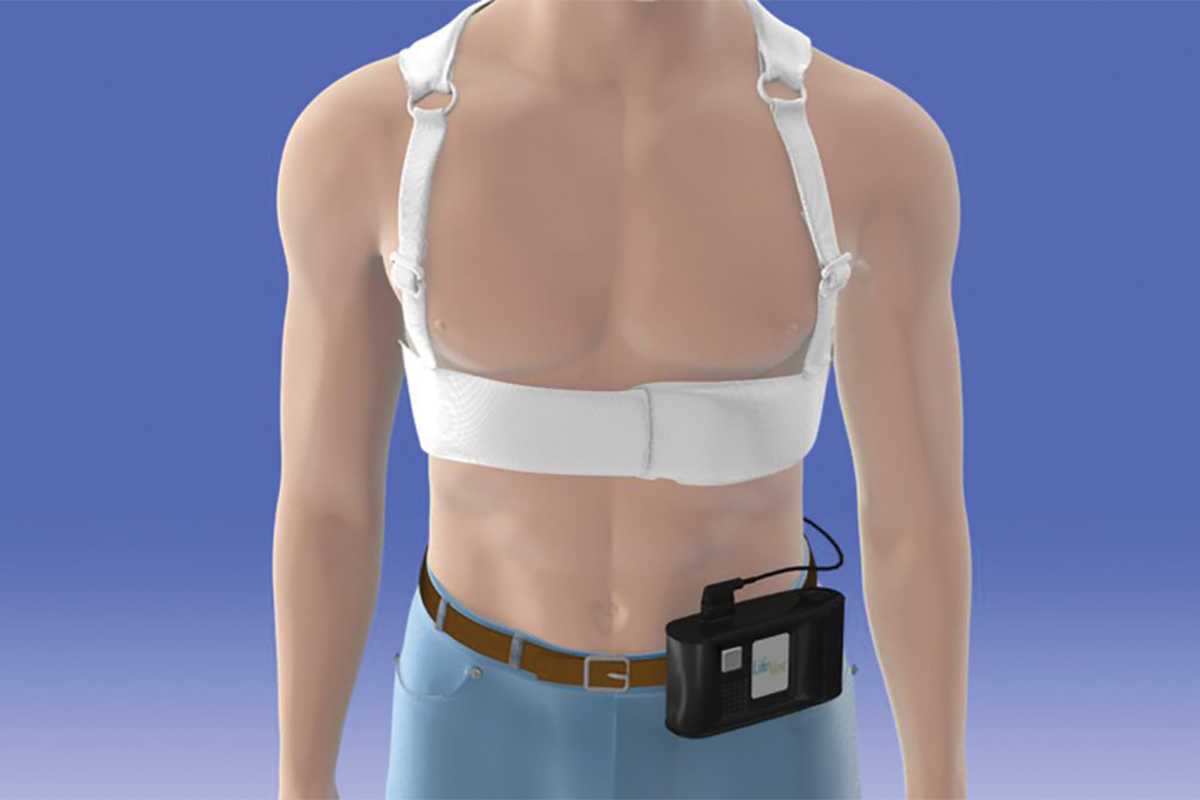
現在利用可能なWCDのバージョンは、Zoll MedicalCorporationのLifeVestです。背中に沿って垂直に配置された2つの除細動器パッドを備えた胸部衣服、心臓のリズムを検出する電極を備えた水平に配置された除細動器パッドを含む前部ベルト、およびリズムを記録してバッテリーを含む小さなモニターボックス。 LifeVestをアクティブにすると、3つのアラームが発生する可能性があります。モニターボックスに注意が必要であることを示すゴングアラート。致命的な不整脈が検出され、WCD治療シーケンスがアクティブになっていることを示す振動アラート。ショックが差し迫っていることを示すサイレンアラート。ショックが発生する直前に、3つの除細動パッドから青いゲルが患者に放出され、電気伝導の接触が改善されます。衝撃的なベクトルは、背面の除細動器パッドと前部ベルトの除細動器パッドの間にあります。
WCDの実際の経験は、2001年から2018年に公開された多数の研究で説明されています。調査された最大の患者コホートには、Zollレジストリからの8,453人の患者が含まれていました。合計で、133人の患者(1.6%)が309の適切なショックを受け、91%のショックが心室性頻脈性不整脈から患者を蘇生させることに成功しました(非血管再生患者で84%、血管再生患者で95%)。 AMIからショックまでの期間の中央値は16日で、ショックの75%はAMIの翌月に発生しました。8
待望のVEST研究は、筆頭著者によって遅発性臨床試験として発表されました。ジェフリーE.オルギン、MD、FACC、ACC.18で、最終的にニューイングランドジャーナルオブメディシンに掲載されました。VEST試験の目標は、MIがあり、LVEFが低下している患者にICDが適応となる前の期間におけるWCDの有効性を判断することでした。ほぼ10年間の登録期間にわたって、この試験では、AMIとLVEFが35%以下の2,302人の患者をWCDとWCDなしの2:1の比率でランダム化しました。分析はITT法で実施されました。
VESTの結果は、突然死または心室頻拍または心室細動による90日での死(不整脈)の主要な複合転帰に有意差がないことで注目に値しました。死亡)、これはWCDグループの患者の1.6%および非WCDグループの患者の2.4%で発生しました(相対リスク、0.66; 95%信頼区間、0.37-121; p = 0.18)。
特に、WCDグループの43人の患者(2.8%)はデバイスを着用したことがなく、非WCDグループの20人の患者(2.6%)は研究外でデバイスを受け取りました。 WCDグループの10人の患者(0.7%)と非WCDグループの15人の患者(1.5%)はフォローアップのために失われ、各グループの2人の患者(合計5%)は突然の原因を特定するのに十分なデータがありませんでした死。著者らは、WCDグループでWCDを着用しなかったことが、試験の最初の2週間で70%の予想WCD着用時間しか達成されなかったため、研究の力を低下させた可能性があることへの懸念を表明した。最終的に、VEST試験は、WCDが対象集団のSCDのリスクを大幅に低減する能力についての否定的な研究と見なされました。2
しかし、否定的な結果はWCDの使用を思いとどまらせるようには見えませんでした。代わりに、研究者にその発見に挑戦するように勧めました。 2001年から2018年までの33,242人の患者(VEST試験の介入群を含む)を対象とした28件の研究で利用可能な最大のメタ分析により、適切なWCD治療、適切なWCDショック、および不適切なWCDショックが7/100人の割合で発生したことが明らかになりました。 、5/100人、および2/100人、それぞれ3か月間。
このメタ分析では、虚血性心筋症、非虚血性心筋症、および混合型心筋症の患者が適切なWCDを経験しました。 3か月の期間にわたって、それぞれ8/100人、6/100人、および3/100人の割合での治療。 VESTの虚血性心筋症の患者と比較して、非VESTコホートの虚血性心筋症の患者は、適切なWCD療法の発生率が高いことを示しました(3か月間で11/100人対1/100人)。 WCD処方のパターンを調べたところ、著者らは、WCDの継続的な使用は、「SCDの最終性と、それを裏付けるデータがないにもかかわらず、訴訟の恐れによって引き起こされている可能性が高い」という興味深い観察を行いました9 p。 >
これらの研究の2つ目は、メディケアの請求データから、16,935人の患者のWCD使用に関連する死亡率と費用を調査しました。 WCDの使用は、AMI後の1年間の死亡率の大幅な減少と関連しており(19.8%対11.5%; p = 0.017)、この絶対死亡率の8.3%の減少は、12,373.11ドルの増分費用対効果比(ICER)に対応しました。言い換えれば、AMI後の最初の年の命を救うためにWCDの使用は12,373ドルかかります。診療ガイドラインとパフォーマンス測定におけるコスト/価値の方法論に関するACC / AHA声明によると、WCDのICERは高価値のリソースとして分類されます(ICER 12
WCDの受け入れへの道のりは遠回りであり、現代の救命医療機器の短いリストの中でその地位を獲得しています。したがって、最新の2017 ACC / AHA / HRSガイドラインでは、LVEFが35%以下の患者でAMIの後にWCDを使用しています。 IIbの推奨事項が与えられています(図2)。5
すべての治療法と同様に、WCDは処方どおりに使用すると最も効果的ですが、これには最大90日間の継続的な遵守と、さまざまなことに常に注意を払う必要があります。いつでも作動する可能性のあるデバイスアラーム衣服、モニター、および全体的な患者体験を改善するための開発が進行中ですが、遵守により、この厄介なデバイスから実際に恩恵を受ける患者人口が制限される可能性があります。 t o心臓専門医は、LifeVestを受け取るだけでなく、それを着用するのに最も適切な候補者を決定します。

この記事は、ニューヨークのマウントシナイメディカルセンターの電気生理学トレーニングフェロー(FIT)であるEdward Chu、MD(@Ed_Chu_MD)によって執筆されました。
- Feldman AM、Klein H、Tchou P、他WearITの調査員およびコーディネーター。 BIROADの調査員およびコーディネーター。突然死のリスクが高い患者の頻脈性不整脈を終わらせるためのウェアラブル除細動器の使用:WEARIT / BIROADの結果。 Pacing Clin Electrophysiol 2004; 27(1):4-9。
- Olgin JE、Pletcher MJ、Vittinghoff E、etal。 VESTInvestigators。心筋梗塞後の装着型除細動器。N Engl J Med 2018; 379:1205-15。
- Hohnloser SH、Kuck KH、Dorian P、et al; DINAMITInvestigators。急性心筋梗塞後の植込み型除細動器の予防的使用。 N Engl J Med 2004; 351:2481-8。
- Steinbeck G、Andresen D、Seidl K、et al; IRIS調査員。心筋梗塞後早期の除細動器の埋め込み。 N Engl J Med 2009; 361:1427-36。
- Al-Khatib SM、Stevenson WG、AckermanMJなど。心室性不整脈患者の管理と心臓突然死の予防に関する2017年のAHA / ACC / HRSガイドライン:エグゼクティブサマリー:米国心臓病学会/米国心臓協会の診療ガイドラインおよび心臓リズム学会のタスクフォースのレポート。 J Am Coll Cardiol 2018; 72:1677-1749。
- Solomon SD、Zelenkofske S、McMurray JJ、他急性心筋梗塞試験(VALIANT)研究者におけるバルサルタン。心筋梗塞および左心室機能不全、心不全、あるいはその両方の患者の突然死。 N Engl J Med 2005; 352:2581-8。
- ZollLifeVest。ゾルメディカルコーポレーション。 2020年9月13日にアクセス。
- エプスタインAE、アブラハムWT、ビアンコNRなど。心筋梗塞後早期にリスクが高いと認識されている患者での装着型除細動器の使用。 J Am Coll Cardiol 2013; 62:2000-7。
- Masri A、Altibi AM、Erqou S、etal。心臓突然死の予防のための装着型除細動器療法:系統的レビューとメタアナリシス。 JACC Clin Electrophysiol 2019; 5:152-61。
- Olgin JE、Lee BK、Vittinghoff E、etal。 VEST試験の結果に対する装着型除細動器コンプライアンスの影響:治療時およびプロトコルごとの分析。 J Cardiovasc Electrophysiol 2020; 31:1009-18。
- Clark MA、Szymkiewicz SJ、Volosin K.急性心筋梗塞後の装着型除細動器に関連する死亡率と費用:メディケア請求データの後ろ向きコホート分析。 J Innov Card Rhythm Manag 2019; 10:3866-73。
- Anderson JL、Heidenreich PA、BarnettPGなど。パフォーマンス測定に関するACC / AHAタスクフォース。実践ガイドラインに関するACC / AHAタスクフォース。臨床診療ガイドラインおよびパフォーマンス測定におけるコスト/価値方法論に関するACC / AHA声明:パフォーマンス測定に関する米国心臓病学会/米国心臓協会タスクフォースおよび診療ガイドラインに関するタスクフォースの報告。 J Am Coll Cardiol 2014; 63:2304-22。
臨床トピック:不整脈および臨床EP、SCD /心室性不整脈
キーワード:ACC Publications、Cardiology Magazine、米国食品医薬品局、デバイス承認、心室細動、発生率、1回拍出量、リスク、信頼区間、メディケア、費用-利益分析、振動、フォローアップ研究、目標、治療分析の意図、フォローアップの喪失、標準的なケア
<リストに戻る