La terapia con cellule T CAR rimodellata riduce gli effetti collaterali nel primo studio clinico
20 febbraio 2020, da personale NCI
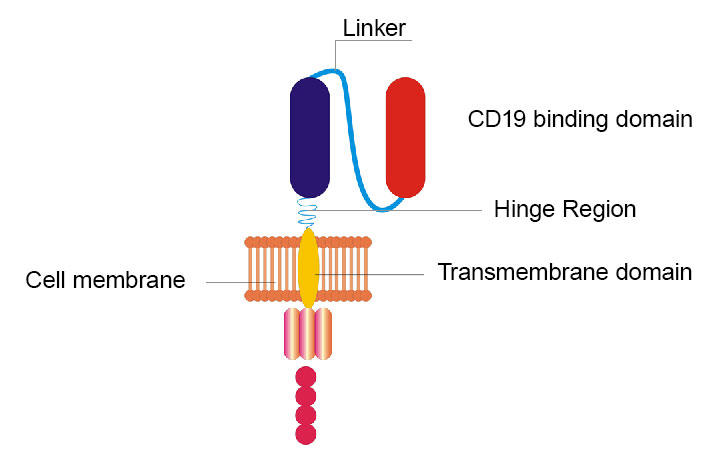
I ricercatori NCI hanno rimodellato il loro CAR CD19 originale sostituendo la cerniera e transmembrana e scambiando il dominio di legame CD19 da un frammento proteico trovato nei topi a un frammento simile trovato negli esseri umani.
Nel corso di diversi decenni, gli scienziati dellNCI hanno gettato le basi per un romanzo trattamento che alla fine sarebbe diventato axicabtagene ciloleucel (Yescarta), una terapia a cellule T CAR per adulti con linfoma.
Sebbene la terapia possa portare a remissioni di lunga durata per alcuni pazienti con cancro molto avanzato, può anche causare effetti collaterali neurologici come problemi di linguaggio, tremori, delirio e convulsioni. Alcuni effetti collaterali possono essere gravi o fatali.
Quindi, nel 2017, i ricercatori dellNCI hanno ottimizzato il loro design originale delle cellule T CAR con lobiettivo di creare una terapia più sicura ed efficace. Ora i risultati del primo studio clinico sui linfociti T CAR rimodellati suggeriscono che potrebbero aver raggiunto parte del loro obiettivo.
La nuova terapia ha causato molti meno effetti collaterali neurologici rispetto alla terapia originale in uno studio precedente, eppure era altrettanto efficace. I risultati sono stati riportati il 20 gennaio su Nature Medicine.
“È straordinario che su 20 pazienti in questo studio, solo uno ha avuto gravi effetti collaterali neurologici”, ha detto il ricercatore associato Jennifer Brudno, MD, del Center for NCI Ricerca sul cancro.
“Questo sembra essere un progresso significativo nella nostra attuale comprensione di come funzionano le cellule T CAR e come creare una CAR T più sicura”, ha affermato David Maloney, MD, Ph.D., medico direttore dellimmunoterapia cellulare per il Fred Hutchinson Cancer Research Center, che non è stato coinvolto nello studio.
Tuttavia, lo studio è limitato dal numero esiguo di pazienti coinvolti e dal periodo relativamente breve di tempo in cui sono stati monitorati i risultati dei pazienti, ha aggiunto.
Le cellule T ottengono una nuova AUTO
La terapia con le cellule T CAR consiste nellarmare le cellule T del paziente (un tipo di globulo bianco) con una proteina specializzata chiamata CAR, o chimerica recettore dellantigene. Questo recettore aiuta le cellule T a trovare e uccidere il cancro della persona.
Lauto rimodellata del team NCI è diversa dalloriginale per alcuni aspetti. Ad esempio, sono state sostituite due sezioni (chiamate domini cerniera e transmembrana) del CAR originale. E unaltra sezione che originariamente consisteva in un frammento proteico trovato nei topi è stata sostituita con un frammento simile trovato negli esseri umani. Ma, come loriginale, il nuovo CAR prende di mira anche il CD19, una molecola che studia la superficie delle cellule di linfoma.
In precedenti studi di laboratorio, i ricercatori hanno scoperto che i linfociti T armati con la nuova CAR rallentavano la crescita dei tumori nei topi. E rispetto alle cellule T CAR originali, le nuove cellule T CAR hanno prodotto livelli inferiori di sostanze chiamate citochine.
Gli scienziati non comprendono appieno come le cellule T CAR causino effetti collaterali neurologici, ma le citochine potrebbero essere parzialmente colpa. Le citochine sono anche il colpevole della sindrome da rilascio di citochine, un altro effetto collaterale potenzialmente letale della terapia con cellule T CAR.
Con questi risultati promettenti, il team è andato avanti con uno studio per la prima volta nelluomo sui linfociti CAR T rimodellati.
Meno citochine, meno effetti collaterali neurologici
Nel nuovo studio, la dottoressa Brudno ei suoi colleghi hanno somministrato la nuova terapia con cellule T CAR a 20 pazienti con linfoma a cellule B.
Complessivamente, quattro pazienti (20%) hanno manifestato una certa tossicità neurologica: tre hanno avuto effetti lievi e uno (5%) ha avuto effetti gravi che sono rapidamente scomparsi dopo il trattamento con uno steroide (medicinale che inibisce il sistema immunitario ).
In uno studio precedente sulla terapia originale con cellule T CAR che coinvolge 22 persone con linfoma a cellule B, 17 (77%) hanno sperimentato una certa tossicità neurologica, inclusi 11 pazienti (50%) che hanno manifestato sintomi gravi.
Due pazienti (10%) nel nuovo studio e quattro (18%) nello studio precedente avevano una sindrome da rilascio di citochine grave. “Sembra favorevole quello simile, ma è difficile dire se è decisamente meno frequente” con la nuova terapia, ha detto il dottor Brudno.
I livelli di citochine erano più bassi nel sangue dei pazienti trattati con la nuova terapia rispetto ai pazienti che hanno ricevuto la terapia originale, hanno scoperto gli scienziati, il che potrebbe spiegare perché la nuova terapia ha causato meno effetti collaterali neurologici, hanno scritto.
In entrambi gli studi, i ricercatori hanno utilizzato gli stessi metodi per valutare la gravità di tossicità neurologica e sindrome da rilascio di citochine, ha osservato il Dr. Brudno.
E sebbene ci siano altre somiglianze tra le due prove – sono state condotte nella stessa struttura, per esempio – è difficile confrontare i risultati di studi indipendenti, ha detto.
Cellule T CAR che restano attaccate
Un problema con le attuali terapie con cellule T CAR è che le cellule non durano molto a lungo nel corpo del paziente. Ciò è in parte dovuto al fatto che il sistema immunitario umano può vedere le proteine del topo come non familiari e distruggere le cellule T CAR.
Parte dellobiettivo del team era creare cellule T CAR che restassero o persistessero più a lungo. Hanno pensato che le cellule T con una CAR composta da tutte le proteine umane potrebbero durare più a lungo delle cellule con una CAR contenente proteine di topo.
Se il sistema immunitario del paziente ignora una CAR composta da proteine umane, le cellule CAR T potrebbero durare più a lungo ed essere più efficaci, ha spiegato il dottor Brudno.
Potrebbe essere il caso per la nuova terapia. Un mese dopo aver ricevuto il trattamento, cerano livelli più alti di cellule T CAR nel sangue dei pazienti che avevano ricevuto la nuova terapia rispetto a quelli trattati con la terapia originale.
Questi risultati sono “incoraggianti” e dovrebbero essere esplorato in studi futuri, ha detto il dottor Maloney.
Sebbene le nuove cellule T CAR sembrino persistere più a lungo delle cellule T CAR originali, non sembravano essere più efficaci. In entrambi gli studi, più della metà (55%) dei partecipanti è andato in remissione completa.
Ma è “incoraggiante” vedere “unottima efficacia per questo prodotto a cellule T CAR, oltre alla bassa tossicità”, ha detto il dott. Brudno ha detto.
Una riprogettazione informativa
La terapia con cellule T CAR può portare a una vasta gamma di effetti neurologici, che vanno da molto lievi a gravi e pericolosi per la vita, ha spiegato il dott. Brudno.
Questi effetti collaterali sono associati a tutte le terapie con cellule T CAR attualmente disponibili, due approvate dalla FDA e unaltra in attesa di approvazione della FDA, ha osservato il dottor Maloney. Udies, i tassi di tossicità neurologica grave variavano dal 5% al 50%.
Altri studi clinici stanno testando terapie con cellule T CAR che sono state anche riprogettate per essere più sicure, ha osservato il dottor Maloney. Il nuovo studio NCI identifica aspetti del design delle cellule T CAR che in precedenza non erano noti per influenzare la tossicità neurologica, ha detto.
“Ma come si traduce questo in un nuovo prodotto commerciale o si aggiorna un prodotto commerciale è una questione completamente diversa”, ha detto. La produzione di una terapia con cellule T CAR per ogni singolo paziente è un processo complesso e costoso che può essere fatto solo presso strutture altamente specializzate.
Per ora, il team NCI, guidato da James Kochenderfer, MD, è concentrato sulla conduzione di studi clinici di diverse terapie con cellule T CAR per persone con un altro tipo di sangue cancro, mieloma multiplo.