Il defibrillatore cardioverter indossabile: una vita (giubbotto) di controversia

Gli Stati Uniti La Food and Drug Administration (FDA) nel 2001 ha approvato un dispositivo medico dopo che il suo principale studio clinico ha dimostrato sicurezza ed efficacia in cinque pazienti su sette che hanno ricevuto cure.1 Per più di un decennio, studi osservazionali nel mondo reale con il dispositivo medico hanno descritto variazioni variabili interpretazioni dellutilità.
Nel 2018, 17 anni dopo lapprovazione della FDA, i risultati del primo studio controllato randomizzato del dispositivo medico hanno rivelato risultati negativi.2 Ad oggi, questo dispositivo medico continua ad essere prescritto e , in alcune istituzioni, è diventato lo standard di cura. Questa è la storia di LifeVest®, lunico defibrillatore cardioverter indossabile approvato dalla FDA (WCD) indicato per ridurre il rischio di morte cardiaca improvvisa (SCD) nei pazienti con frazione di eiezione ventricolare sinistra ridotta (LVEF) che hanno subito un infarto miocardico acuto (AMI).
Il ruolo di un ICD nellimmediato post-IMA in pazienti con una LVEF ≤35-40% è stato precedentemente esplorato in due studi randomizzati controllati (DINAMIT e IRIS) .3, 4 In DINAMIT, cera un tasso significativamente più basso di SCD nei pazienti randomizzati a ICD rispetto a nessun ICD (4% vs 8%; p = 0,009), ma cera un tasso significativamente più alto di morti non SCD nel gruppo ICD rispetto nel gruppo senza ICD (15% vs. 9%; p = 0,02). Allo stesso modo in IRIS, cera un tasso significativamente più basso di SCD nei pazienti randomizzati a ICD rispetto a nessun ICD (6% vs 13%; p = 0,049), ma cera un tasso significativamente più alto di decessi non SCD nel gruppo ICD rispetto nel gruppo senza ICD (15% vs. 9%; p = 0,001).
Sebbene gli ICD fossero associati a un minor rischio di SCD in questi studi randomizzati, ciò è stato compensato dallassociazione con un rischio elevato di eventi non SCD. Di conseguenza, le attuali linee guida dellACC / AHA / HRS raccomandano limpianto di ICD per la prevenzione primaria della SCD in questa popolazione dopo un periodo di 40 giorni di terapia medica diretta dalle linee guida (o 90 giorni di terapia medica diretta dalle linee guida se la rivascolarizzazione è eseguita) (Figura 1) .5
Figura 1: Prevenzione primaria della SCD in pazienti con cardiopatia ischemica
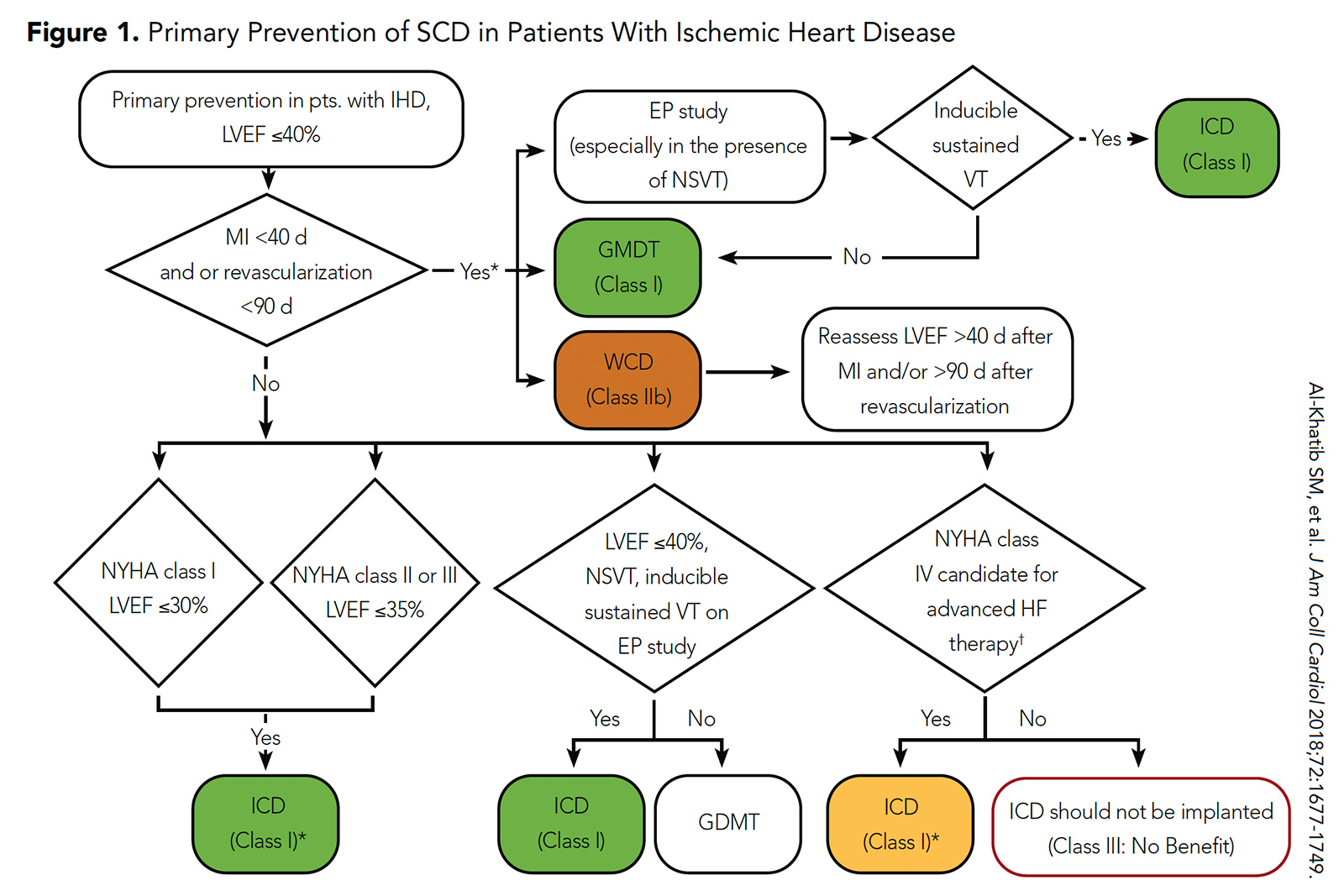 Fare clic sullimmagine sopra per ingrandirla.
Fare clic sullimmagine sopra per ingrandirla. Figura 2: Linee guida ACC / AHA / HRS 2017 per luso del defibrillatore cardioverter indossabile
 Fare clic sullimmagine sopra per ingrandirla.
Fare clic sullimmagine sopra per ingrandirla.
Tuttavia, il rischio di SCD nel periodo immediatamente successivo allAMI è massimo nei primi 30 giorni. Lo studio VALIANT ha arruolato 14.609 pazienti con una LVEF ≤40% dopo IMA e ha dimostrato che il 7% dei pazienti ha subito morte improvvisa o arresto cardiaco durante un periodo di follow-up di due anni. Un allarmante 19% di questi decessi si è verificato nei primi 30 giorni dopo lAMI e il rischio era più alto nei pazienti con una LVEF ≤30% (2,3% al mese) .6
Considerati insieme ai risultati di DINAMIT e IRIS, i risultati di VALIANT hanno indicato la necessità di una strategia non-ICD per proteggere i pazienti dal verificarsi di SCD. Il WCD, che era già stato approvato dalla FDA al momento di queste prove, sembrava essere la soluzione perfetta.
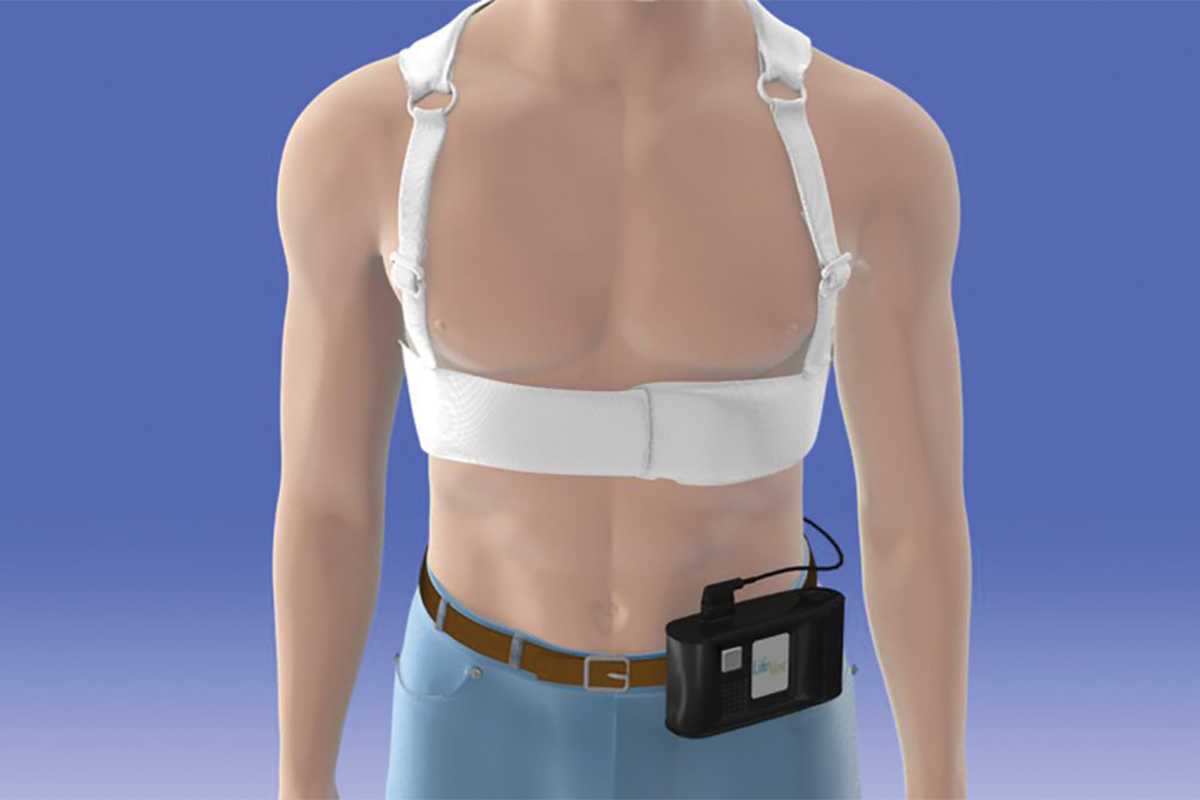
La versione attualmente disponibile del WCD è il LifeVest di Zoll Medical Corporation.7 Il dispositivo è costituito da un indumento toracico con due pad defibrillatori posizionati verticalmente lungo la schiena, una cintura frontale contenente un pad defibrillatore posizionato orizzontalmente con elettrodi che rilevano il ritmo cardiaco e una piccola scatola monitor che registra i ritmi e contiene la batteria. Una volta attivato, LifeVest può fornire al paziente tre possibili allarmi: un allarme gong che indica che è richiesta attenzione alla scatola del monitor; un avviso di vibrazione che indica che è stata rilevata unaritmia letale e che la sequenza di trattamento WCD è in corso; e un allarme sirena che indica che uno shock è imminente. Immediatamente prima dellerogazione della scarica, un gel blu viene rilasciato dai tre elettrodi di defibrillazione sul paziente per migliorare il contatto per la conduzione elettrica. Il vettore scioccante si trova tra gli elettrodi del defibrillatore sul retro e gli elettrodi del defibrillatore nella cintura frontale.
Lesperienza del mondo reale con il WCD è stata descritta in numerosi studi pubblicati dal 2001 al 2018. Uno dei le più grandi coorti di pazienti studiate includevano 8.453 pazienti del registro Zoll. In totale, 133 pazienti (1,6%) hanno ricevuto 309 shock appropriati con il 91% degli shock che hanno rianimato con successo il paziente da una tachiaritmia ventricolare (84% nei pazienti non rivascolarizzati e 95% nei pazienti rivascolarizzati). Il tempo mediano dallAMI allo shock è stato di 16 giorni e il 75% degli shock si è verificato nel mese successivo allAMI.8
Il tanto atteso studio VEST è stato presentato dallautore principale come una sperimentazione clinica ritardata Jeffrey E. Olgin, MD, FACC, allACC.18, e infine pubblicato sul New England Journal of Medicine.Lobiettivo dello studio VEST era di determinare lefficacia del WCD durante il periodo prima che gli ICD fossero indicati nei pazienti che hanno avuto un IM e hanno una LVEF ridotta. In un periodo di arruolamento di quasi dieci anni, lo studio ha randomizzato 2.302 pazienti con IMA e una LVEF ≤35% in un rapporto 2: 1 rispetto a WCD rispetto a nessun WCD. Lanalisi è stata condotta in modo intent-to-treat.
I risultati del VEST sono stati notevoli per nessuna differenza significativa nelloutcome composito primario di morte improvvisa o morte per tachicardia ventricolare o fibrillazione ventricolare a 90 giorni (aritmica morte), che si è verificata nell1,6% dei pazienti nel gruppo WCD e nel 2,4% dei pazienti nel gruppo non WCD (rischio relativo, 0,66; intervallo di confidenza 95%, 0,37-121; p = 0,18).
In particolare, 43 pazienti (2,8%) nel gruppo WCD non hanno mai indossato un dispositivo e 20 pazienti (2,6%) nel gruppo non WCD hanno ricevuto il dispositivo al di fuori dello studio; 10 pazienti nel gruppo WCD (0,7%) e 15 pazienti nel gruppo non WCD (1,5%) sono stati persi al follow-up e due pazienti in ciascun gruppo (5% totale) non avevano dati sufficienti per determinare la causa dellimprovviso Morte. Gli autori hanno espresso la preoccupazione che la non aderenza di indossare il WCD nel gruppo WCD possa aver ridotto la potenza dello studio, poiché il tempo di usura previsto del WCD del 70% è stato raggiunto solo nelle prime due settimane dello studio. In definitiva, lo studio VEST è stato visto come uno studio negativo per la capacità del WCD di ridurre significativamente il rischio di SCD nella sua popolazione target.2
Tuttavia, i risultati negativi non sembrano dissuadere luso del WCD e ha invece incoraggiato i ricercatori a sfidare i suoi risultati. La più ampia meta-analisi disponibile di 28 studi con 33.242 pazienti (incluso il braccio interventistico dello studio VEST) dal 2001 al 2018 ha rivelato che trattamenti WCD appropriati, shock WCD appropriati e shock WCD inappropriati si sono verificati a un tasso di 7/100 persone , 5/100 persone e 2/100 persone, rispettivamente, per un periodo di tempo di tre mesi.
In questa meta-analisi, i pazienti con cardiomiopatia ischemica, cardiomiopatia non ischemica e cardiomiopatia mista hanno sperimentato una WCD appropriata trattamenti a un ritmo di 8/100 persone, 6/100 persone e 3/100 persone, rispettivamente, su un periodo di tre mesi. Rispetto ai pazienti con cardiomiopatia ischemica nel VEST, i pazienti con cardiomiopatia ischemica nella coorte non VEST hanno dimostrato una maggiore incidenza di una terapia WCD appropriata (11/100 persone contro 1/100 persone nellarco di tre mesi). Nellesaminare il modello di prescrizione di WCD, gli autori hanno fatto linteressante osservazione che luso in corso di WCD “è probabilmente guidato dalla finalità della SCD e in parte dalla paura del contenzioso, nonostante lassenza di dati a supporto.” 9
Il secondo di questi studi ha esaminato la mortalità e i costi associati alluso di WCD in 16.935 pazienti dai dati sulle richieste di assistenza Medicare. Luso della WCD è stato associato a una riduzione significativa della mortalità a un anno dopo lAMI (19,8% contro 11,5%; p = 0,017), e questa riduzione dell8,3% della mortalità assoluta corrispondeva a un rapporto costi-efficacia incrementale (ICER) di $ 12.373,11 In altre parole, luso del WCD costa $ 12.373 per salvare una vita nel primo anno dopo lAMI. Secondo la dichiarazione ACC / AHA sulla metodologia costo / valore nelle linee guida di pratica clinica e nelle misure di prestazione, lICER per il WCD sarebbe classificato come una risorsa di alto valore (ICER 12
Sebbene il viaggio per laccettazione del WCD abbia stato tortuoso, si è guadagnato il suo posto nella breve lista dei moderni dispositivi medici salvavita. Di conseguenza, nelle più recenti linee guida ACC / AHA / HRS 2017, luso di un WCD dopo lAMI in pazienti con una LVEF ≤35% ha è stata data una raccomandazione IIb (Figura 2) .5
Come tutte le terapie, il WCD è più efficace se usato come prescritto, ma ciò richiede unaderenza continua fino a 90 giorni oltre a unattenzione costante verso i vari allarmi del dispositivo che possono attivarsi in un dato momento. Sono in corso sviluppi per migliorare gli indumenti, i monitor e lesperienza complessiva del paziente, ma laderenza limiterà probabilmente la popolazione di pazienti che trarrà effettivamente vantaggio da questo ingombrante dispositivo. Nel frattempo, rimarrà attiva t o il cardiologo per decidere quali pazienti sono i candidati più appropriati non solo per ricevere il LifeVest, ma anche per indossarlo.

Questo articolo è stato scritto da Edward Chu, MD, (@Ed_Chu_MD), elettrofisiologia Fellow in Training (FIT) presso il Mount Sinai Medical Center di New York.
- Feldman AM, Klein H, Tchou P, et al. Investigatori e coordinatori di WEARIT; Investigatori e coordinatori di BIROAD. Uso di un defibrillatore indossabile per porre fine alle tachiaritmie in pazienti ad alto rischio di morte improvvisa: risultati del WEARIT / BIROAD. Pacing Clin Electrophysiol 2004; 27 (1): 4-9.
- Olgin JE, Pletcher MJ, Vittinghoff E, et al. Investigatori VEST. Defibrillatore cardioverter indossabile dopo infarto miocardico.N Engl J Med 2018; 379: 1205-15.
- Hohnloser SH, Kuck KH, Dorian P, et al; Investigatori DINAMIT. Uso profilattico di un defibrillatore cardioverter impiantabile dopo infarto miocardico acuto. N Engl J Med 2004; 351: 2481-8.
- Steinbeck G, Andresen D, Seidl K, et al; Investigatori IRIS. Impianto del defibrillatore subito dopo linfarto del miocardio. N Engl J Med 2009; 361: 1427-36.
- Al-Khatib SM, Stevenson WG, Ackerman MJ, et al. Linee guida AHA / ACC / HRS 2017 per la gestione dei pazienti con aritmie ventricolari e la prevenzione della morte cardiaca improvvisa: Riepilogo esecutivo: A Report of the American College of Cardiology / American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. J Am Coll Cardiol 2018; 72: 1677-1749.
- Solomon SD, Zelenkofske S, McMurray JJ, et al. Valsartan nella sperimentazione sullinfarto miocardico acuto (VALIANT). Morte improvvisa in pazienti con infarto miocardico e disfunzione ventricolare sinistra, insufficienza cardiaca o entrambi. N Engl J Med 2005; 352: 2581-8.
- Zoll LifeVest. Zoll Medical Corporation. Disponibile qui Accesso 13 settembre 2020.
- Epstein AE, Abraham WT, Bianco NR, et al. Uso di defibrillatore cardioverter indossabile in pazienti percepiti come ad alto rischio post-infarto miocardico precoce. J Am Coll Cardiol 2013; 62: 2000-7.
- Masri A, Altibi AM, Erqou S, et al. Terapia con defibrillatore cardioverter indossabile per la prevenzione della morte cardiaca improvvisa: una revisione sistematica e una meta-analisi. JACC Clin Electrophysiol 2019; 5: 152-61.
- Olgin JE, Lee BK, Vittinghoff E, et al. Impatto della conformità del defibrillatore cardioverter indossabile sui risultati nello studio VEST: analisi trattate come e per protocollo. J Cardiovasc Electrophysiol 2020; 31: 1009-18.
- Clark MA, Szymkiewicz SJ, Volosin K. Mortalità e costi associati ai defibrillatori cardioverter indossabili dopo infarto miocardico acuto: unanalisi di coorte retrospettiva dei dati delle richieste di assistenza Medicare. J Innov Card Rhythm Manag 2019; 10: 3866-73.
- Anderson JL, Heidenreich PA, Barnett PG, et al; Task Force ACC / AHA sulle misure di prestazione; Task Force ACC / AHA sulle linee guida pratiche. Dichiarazione ACC / AHA sulla metodologia costo / valore nelle linee guida della pratica clinica e nelle misure delle prestazioni: un rapporto della Task Force dellAmerican College of Cardiology / American Heart Association sulle misure delle prestazioni e della Task Force sulle linee guida pratiche. J Am Coll Cardiol 2014; 63: 2304-22.
Argomenti clinici: Aritmie e EP clinico, SCD / aritmie ventricolari
Parole chiave: Pubblicazioni ACC, Rivista di cardiologia, Food and Drug Administration degli Stati Uniti, Approvazione del dispositivo, Fibrillazione ventricolare, Incidenza, Volume di ictus, Rischio, Intervalli di fiducia, Medicare, Costo -Benefit Analysis, Vibration, Follow-Up Studies, Goals, Intention to Treat Analysis, Lost to Follow-Up, Standard of Care
< Torna agli elenchi