Remodelovaná terapie T-buňkami CAR snižuje vedlejší účinky v první klinické studii
20. února 2020, zaměstnanci NCI
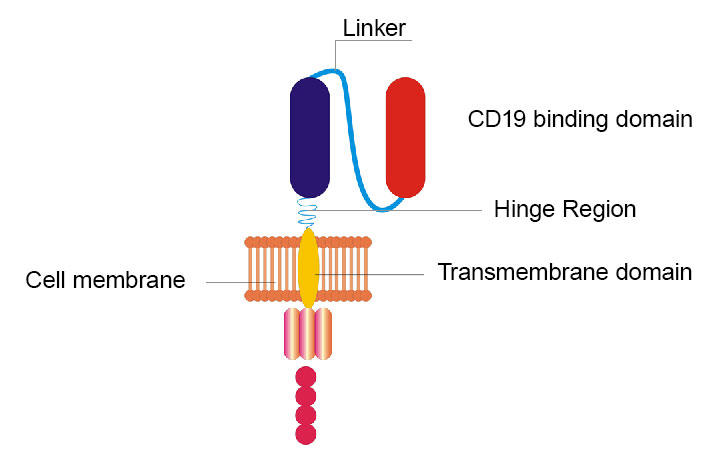
Vědci NCI předělali původní CD19 CAR výměnou závěsu a transmembránové domény a výměna vazebné domény CD19 z proteinového fragmentu nalezeného u myší za podobný fragment nalezený u lidí.
V průběhu několika desetiletí položili vědci NCI rozsáhlé základy románu léčba, která by se nakonec stala axicabtagene ciloleucel (Yescarta), terapií T-buňkami CAR pro dospělé s lymfomem.
I když terapie může u některých pacientů s velmi pokročilým nádorovým onemocněním vést k dlouhodobé remisi, může také způsobit neurologické vedlejší účinky, jako jsou řeči, třes, delirium a záchvaty. Některé vedlejší účinky mohou být závažné nebo smrtelné.
Takže v roce 2017 vědci NCI vylepšili svůj původní design CAR T-buněk s cílem vytvořit bezpečnější a efektivnější terapii. Výsledky první klinické studie remodelovaných CAR T buněk naznačují, že mohly dosáhnout části svého cíle.
Nová léčba způsobila mnohem méně neurologických vedlejších účinků než původní léčba v dřívější studii, přesto to bylo stejně účinné. Nálezy byly hlášeny 20. ledna v Nature Medicine.
„Je pozoruhodné, že z 20 pacientů v této studii měl pouze jeden závažné neurologické vedlejší účinky,“ uvedla MD, odborná spolupracovnice Jennifer Brudno, z Centra pro NCI. Cancer Research.
„Zdá se, že jde o významný pokrok v našem současném chápání toho, jak fungují buňky CAR T a jak zajistit bezpečnější CAR T,“ řekl David Maloney, MD, Ph.D., lékař ředitel buněčné imunoterapie pro Fred Hutchinson Cancer Research Center, který se studie nezúčastnil.
Studie je však omezena malým počtem zúčastněných pacientů a relativně krátkým časovým sledováním výsledků pacientů, dodal.
T buňky získají nový CAR
Terapie T buňkami CAR zahrnuje vyzbrojení pacientových vlastních T buněk (typ bílých krvinek) specializovaným proteinem zvaným CAR nebo chimérickým receptor antigenu. Tento receptor pomáhá T buňkám najít a zabít rakovinu člověka.
Přestavěné CAR týmu NCI se od původního liší několika způsoby. Například byly nahrazeny dvě sekce (nazývané pantové a transmembránové domény) původního CAR. A další část, která původně sestávala z proteinového fragmentu nalezeného u myší, byla vyměněna za podobný fragment nalezený u lidí. Ale stejně jako originál se nový CAR zaměřuje také na CD19, molekulu, která studuje povrch buněk lymfomu.
V dřívějších laboratorních studiích vědci zjistili, že T buňky vyzbrojené novým CAR zpomalily růst nádorů u myší. A ve srovnání s původními CAR T buňkami produkovaly nové CAR T buňky nižší hladiny látek zvaných cytokiny.
Vědci plně nerozumí tomu, jak CAR T buňky způsobují neurologické vedlejší účinky, ale cytokiny mohou být částečně obviňovat. Cytokiny jsou také viníkem syndromu uvolnění cytokinů, což je další potenciálně život ohrožující vedlejší účinek terapie CAR T-buňkami.
S těmito slibnými výsledky se tým posunul vpřed se studií remodelovaných CAR T buněk u člověka.
Méně cytokinů, méně neurologických vedlejších účinků
V nové studii Dr. Brudno a její kolegové poskytli novou terapii T-buňkami CAR 20 pacientům s B-buněčným lymfomem.
Celkově se u čtyř pacientů (20%) vyskytla určitá neurologická toxicita: Tři měli mírné účinky a jeden (5%) zaznamenal závažné účinky, které rychle odezněly po léčbě steroidy (lék, který narušuje imunitní systém) ).
V dřívější studii původní terapie CAR T-buňkami zahrnující 22 lidí s B-buněčným lymfomem došlo u 17 (77%) k neurologické toxicitě – včetně 11 pacientů (50%), u kterých došlo k závažným příznakům.
Dva pacienti (10%) v nové studii a čtyři (18%) v dřívější studii měli syndrom těžkého uvolnění cytokinů. „Zdá se příznivé, že podobné, ale je těžké říci, zda je rozhodně méně časté“ s novou terapií, řekl Dr. Brudno.
Hladiny cytokinů byly nižší v krvi pacientů léčených novou terapií než u pacientů, kteří dostali původní terapii, našli vědci, což by mohlo vysvětlit, proč nová terapie způsobila méně neurologických vedlejších účinků, napsali.
V obou studiích vědci použili stejné metody k hodnocení závažnosti neurologické toxicity a syndromu uvolnění cytokinů, uvedl Dr. Brudno.
A ačkoli existují dvě podobnosti mezi oběma zkouškami – byly prováděny například ve stejném zařízení – je podle ní obtížné porovnávat výsledky nezávislých studií.
CAR T buňky, které se drží kolem
Jedním problémem současných terapií CAR T-buněk je, že buňky nevydrží v těle pacienta příliš dlouho. Je to částečně proto, že lidský imunitní systém vidí myší proteiny jako neznámé a ničí T-buňky CAR.
Součástí cíle týmu bylo vytvořit CAR T buňky, které se budou držet déle nebo přetrvávají. Usoudili, že T buňky s CAR vyrobené ze všech lidských proteinů mohou trvat déle než buňky s CAR obsahujícími myší proteiny.
Pokud imunitní systém pacienta ignoruje CAR vyrobený z lidských proteinů, pak by CAR T buňky mohly trvat déle a být efektivnější, vysvětlil Dr. Brudno.
Může tomu tak být pro novou terapii. Měsíc po léčbě byl u pacientů, kteří dostali novou terapii, vyšší hladiny CAR T buněk v krvi než u pacientů léčených původní terapií.
Tyto nálezy jsou „povzbudivé“ a měly by být zkoumané v budoucích studiích, řekl Dr. Maloney.
Ačkoli se zdá, že nové buňky CAR T přetrvávají déle než původní buňky CAR T, nezdá se, že by byly účinnější. V obou studiích více než polovina (55%) účastníků šlo do úplné remise.
Je však „povzbudivé“ vidět „velmi dobrou účinnost tohoto produktu CAR T-buněk, kromě nízké toxicity,“ Dr. Brudno řekl.
Informativní redesign
Terapie T-buňkami CAR může vést k rozmanité škále neurologických účinků, od velmi mírných až po závažné a život ohrožující, vysvětlil Dr. Brudno.
Tyto vedlejší účinky jsou spojeny se všemi aktuálně dostupnými terapiemi T-buňkami CAR – dvěma, které jsou schváleny FDA a dalšími, které čekají na schválení FDA – poznamenal Dr. Maloney. Míra závažné neurologické toxicity se pohybovala v rozmezí od 5% do 50%.
Další klinické studie testují terapie T-buňkami CAR, které byly také přepracovány tak, aby byly bezpečnější, poznamenal Dr. Maloney. Nová studie NCI identifikuje aspekty designu CAR T-buněk, o kterých nebylo dříve známo, že by ovlivňovaly neurologickou toxicitu, řekl.
„Ale jak to přeložit na nový komerční produkt nebo upgradovat komerční produkt, je úplně jiná otázka,“ řekl. Výroba terapie T-buňkami CAR pro každého jednotlivého pacienta je složitý a nákladný proces, který lze provést pouze ve vysoce specializovaných zařízeních.
Prozatím se tým NCI pod vedením Jamese Kochenderfera zaměřuje na provádění klinických studií různých terapií T-buňkami CAR u lidí s jiným typem krve rakovina, mnohočetný myelom.